2025년 면역세포 치료 최근 연구 결과
페이지 정보
작성자 PnH 조회74회 작성일 25-03-31 19:13본문
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy)는 키메라 항원 수용체 T 세포 면역 요법 입니다 . 이 치료법은 수년 동안 사용되어 온 새로운 유형의 세포 치료법이지만 최근 몇 년 동안에야 연구발전되어 임상에 사용되고 있습니다. 이 약물은 급성 백혈병 과 비호지킨 림프종 치료에 상당한 치료 효과를 가지고 있으며 가장 유망한 종양 치료법 중 하나 입니다 . 모든 기술과 마찬가지로 CAR-T 기술도 긴 진화 과정을 거쳤습니다. 이러한 일련의 진화 과정에서 CAR-T 기술이 점차 견고해졌습니다.
이 새로운 치료 전략의 핵심은 표적 세포를 인식하는 키메라 항원 수용체(CAR)라는 인공 수용체이며, 유전적으로 변형된 후 환자의 T 세포가 이 CAR을 발현할 수 있게 됩니다. 인간을 대상으로 한 임상 실험에서 과학자들은 투석과 유사한 과정을 통해 환자로부터 일부 T 세포를 추출한 다음 실험실에서 유전자 변형을 통해 이 CAR을 인코딩하는 유전자를 도입하여 이들 T 세포가 이 새로운 수용체를 발현할 수 있도록 했습니다. 이렇게 유전자 변형된 T세포는 실험실에서 확장된 후 환자에게 다시 주입됩니다. T 세포는 자신이 발현하는 CAR 수용체를 사용하여 표적 세포 표면의 분자에 결합하고, 이 결합은 내부 신호를 유발하여 T 세포를 매우 강력하게 활성화시켜 표적 세포를 빠르게 파괴합니다.
최근 들어 CAR-T 면역 치료법은 급성 백혈병과 비호지킨 림프종을 치료하는 데 사용되는 것 외에도 연구되어 고형 종양, 자가면역 질환, HIV 감염, 심장병 및 기타 질병을 치료하는 데 사용되어 왔으며 적용 범위가 더 넓어졌습니다. 이를 바탕으로 편집자는 CAR-T 세포 치료 분야에서 이루어진 최신 진전을 파악했습니다!
1. 네이쳐 : 임상 시험에서 GD2를 표적으로 하는 CAR-T 세포가 diffuse intrinsic pontine glioma, DIPG을 치료할 것으로 예상됩니다
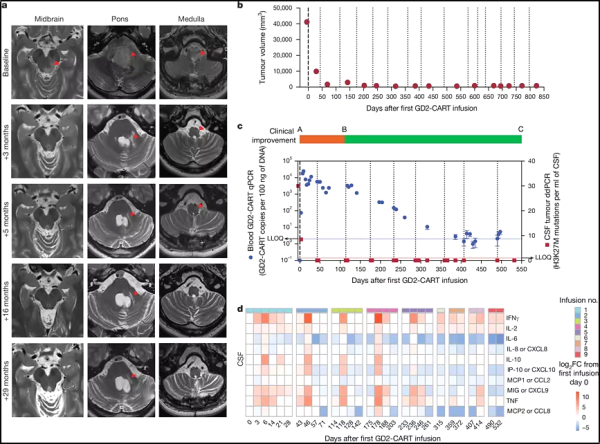
새로운 연구에 따르면, 면역 세포 치료를 통해 어린이의 뇌종양이 줄어들고, 신경 기능이 회복되었으며, 스탠포드 대학 의과대학에서 실시한 임상 실험에 참여한 한 명의 경우 일반적으로 치료가 불가능하다고 여겨지는 뇌암 의 모든 흔적이 사라진 것으로 나타났습니다 . 임상 시험은 CAR-T 세포라는 공학적 면역 세포를 고형 종양을 치료하는 데 성공적으로 사용한 최초의 사례 중 하나로 , (diffuse intrinsic pontine glioma, DIPG)이라는 유형의 암을 포함한 치명적인 뇌 및 척수 종양을 앓고 있는 어린이에게 희망을 안겨줍니다.
2024년 10월, 이 CAR-T 세포 면역 치료법은 미국 식품의약국 ( FDA )으로부터 재생 의학 첨단 치료법 지정을 받았으며, 이를 통해 저자는 FDA 승인 절차의 신속 버전에 참여할 수 있었습니다.
CAR-T 세포 치료를 받은 11명의 참가자 중 9명이 이로부터 효과를 얻었습니다. 9명은 질병으로 인한 장애가 기능적으로 개선되었습니다. 4명의 종양 부피가 절반 이상 줄었습니다. 네 명의 참가자 중 한 명은 완전 반응을 보였습니다. 즉, 뇌 스캔에서 종양이 사라졌습니다. 그가 회복되었는지 말하기에는 너무 이르지만, 그는 진단을 받은 지 4년이 지난 지금도 건강을 유지하고 있습니다.
"이것은 보편적으로 치명적인 질병이며, 우리는 종양을 상당히 줄이고 임상 증상을 개선할 수 있는 치료법을 발견했습니다." 스탠포드 대학교 의대의 소아 신경종양학과 교수이자 논문의 공동 수석 저자인 미셸 몬제 박사가 말했습니다. "각 환자에 대한 치료를 최적화하기 위해서는 아직 갈 길이 멀지만, 한 환자가 완전한 반응을 보였다는 것은 매우 흥미로운 일입니다. 그가 완치되기를 바랍니다."
이 임상 시험에서 사용된 CAR-T 세포 치료법은 스탠포드 대학교 의과대학에서 개발했습니다. 2018년, 몬제의 팀은 DIPG와 기타 확산성 중앙선 신경교종 종양 세포가 GD2라는 표면 마커를 대량으로 생성한다는 것을 발견했습니다. 맥캘의 팀은 일부 다른 암에서도 발견되는 GD2를 표적으로 삼는 CAR-T 세포를 설계했습니다. 그들은 GD2를 표적으로 삼는 CAR-T 세포가 동물 모델에서 DIPG 종양을 근절할 수 있다는 것을 발견했습니다.
새로운 연구에서는 척수의 DIPG 또는 확산성 중앙선 신경교종 환자를 대상으로 진행 중인 임상 시험에 등록한 최초 13명의 환자에 대한 보고가 나와 있습니다. 참가자의 중앙 연령은 15세였고, 시험에 참여하기 전 암 진단의 중앙 기간은 5개월이었습니다. 그중 10명은 DIPG를 앓고 있었고 3명은 척수의 확산성 중앙선 신경교종을 앓고 있었습니다. (참가자 2명의 종양이 너무 빨리 진행되어 CAR-T 세포 치료를 받기 전에 연구에서 실격 처리되었습니다.)
2.Nature:Interleukin-15-armoured GPC3 CAR T cells for patients with solid cancers
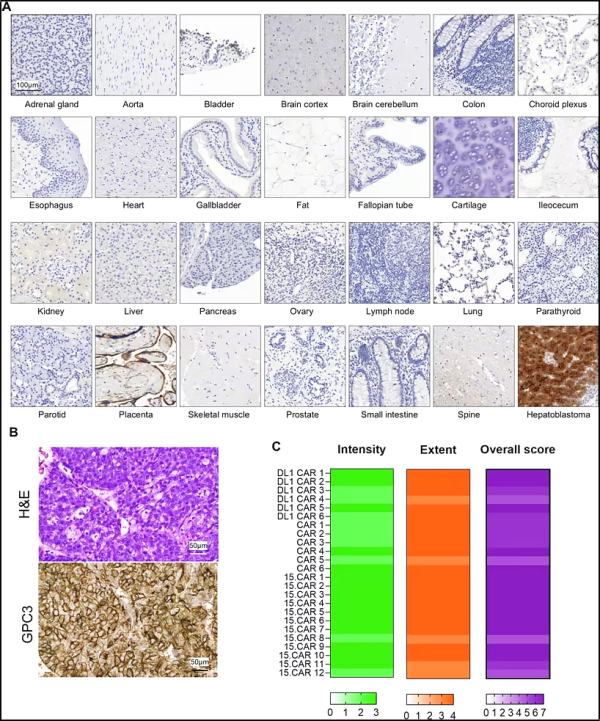
새로운 연구에서 베일러 의과대학과 텍사스 어린이 암 센터의 연구자들은 글리피칸-3(GPC3)를 발현하는 고형 종양을 표적으로 하는 새로운 면역 요법에 대한 최초의 인간 대상 1상 임상 시험 결과를 보고했습니다. 그들은 인터루킨-15(IL-15) 단백질로 강화된 키메라 항원 수용체(CAR) T 세포를 테스트했습니다. 관련 연구 결과는 최근 "고형암 환자를 위한 인터루킨-15- GPC3 CAR T 세포" 라는 제목으로 저널 Nature 에 게재되었습니다.
GPC3 발현 평가: GPC3 발현을 검출하기 위한 면역조직화학
일부 혈액 악성 종양 에서는 큰 성공을 거두었지만 , CAR-T 세포는 고형 종양 환자에게는 효능이 제한적입니다. 전임상 연구에 따르면 T 세포의 생존과 증식에 도움이 되는 IL-15를 추가하면 CAR-T 세포 기반 면역 요법의 효과를 높일 수 있는 것으로 나타났습니다.
이 임상 시험에서 저자들은 간세포암(HCC)을 앓고 있는 성인 환자(NCT02905188)와 GPC3를 발현하는 고형 종양(HCC 포함)을 앓고 있는 소아 환자(NCT02932956)에서 IL-15를 공동 발현하는 GPC3 특이적 CAR-T 세포(이하 GPC3-CAR T 세포)를 테스트했습니다. 첫 번째 환자 그룹은 GPC3-CAR T세포 치료만을 받았습니다. 연구진은 GPC3-CAR T 세포가 안전하다는 것을 발견했으며, 주입 후 2주 만에 세포 증식이 최고조에 달했지만, 객관적인 항암 반응은 관찰되지 않았습니다.
IL-15를 갖춘 GPC3-CAR T 세포는 두 번째 환자 그룹에서 평가되었는데, 이 그룹에도 GPC3를 발현하는 고형 종양이 있는 성인(NCT05103631)과 어린이(NCT04377932)가 포함되었습니다. 이 시험에 참여한 환자들은 CAR T 세포 확장이 상당히 증가했고, 피험자의 33%(4/12)가 객관적인 항종양 반응을 경험했으며, 피험자의 66%(8/12)가 최소 4주 동안 질병이 안정적이었습니다. IL-15가 장착된 GPC3-CAR T 세포로 치료받은 환자는 사이토카인 방출 증후군이 자주 발생했는데, 이는 IL-1/IL-6 차단으로 조절되거나 유도성 카스파제 9 안전 스위치 활성화로 빠르게 개선되었습니다.
비반응자와 비교했을 때, 반응자의 종양 침윤 GPC3-CAR T 세포는 SWI/SNF 후생유전적 조절자의 억제, FOS 및 JUN 패밀리 구성원의 상향 조절, 1형 인터페론 신호 전달에 관여하는 유전자의 상향 조절을 보였습니다. 이러한 결과는 IL-15가 환자 GPC3 CAR T 세포의 증식, 종양 내 생존 및 항종양 활동을 향상시킬 수 있음을 시사합니다.
3. Cell Stem Cell:Patient-derived glioblastoma organoids as real-time avatars for assessing responses to clinical CAR-T cell therapy.
신경교종(GBM)은 성인에서 가장 흔하고 공격적인 암성 뇌종양입니다. GBM 환자는 보통 진단 후 12~18개월만 생존합니다. 수십 년간의 연구에도 불구하고 GBM을 치료할 수 있는 방법은 알려지지 않았으며, 수술, 방사선 치료, 화학 요법과 같은 승인된 치료법은 기대 수명을 연장하는 데 효과가 제한적입니다.
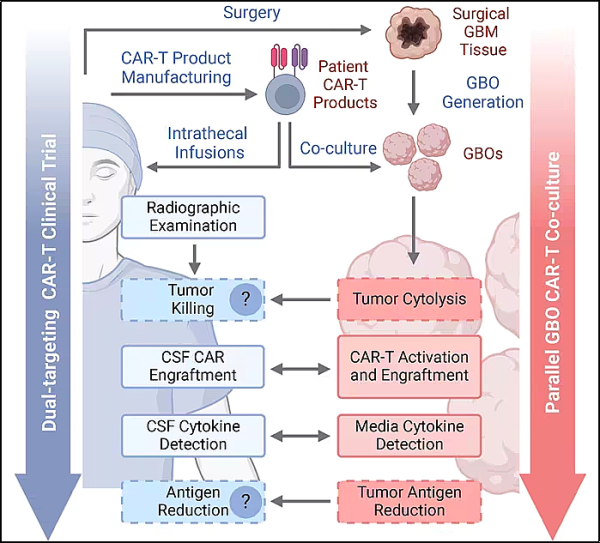
펜실베이니아 대학의 연구자들은 새로운 연구에서 GBM 환자에게서 유래한 종양에서 만든 실험실에서 배양한 오르가노이드를 처음으로 사용하여 CAR-T 세포 치료에 대한 환자의 반응을 실시간으로 정확하게 시뮬레이션했습니다. 오르가노이드가 치료에 반응하는 모습은 환자 뇌의 실제 종양과 유사했습니다. 즉, 종양에서 유래된 기관체가 치료 후에 줄어들면 환자의 실제 종양도 줄어들 것입니다. 관련 연구 결과는 2024년 12월 9일 "임상 CAR-T 세포 치료에 대한 반응을 평가하기 위한 실시간 아바타로서의 환자 유래 신경교종 기관소체" 라는 제목으로 저널 Cell Stem Cell 에 온라인으로 게재되었습니다.
"GBM 환자가 치료에 어떻게 반응하는지 측정하기는 어렵습니다. 뇌를 정기적으로 생검할 수 없고 MRI를 기준으로 종양 성장과 치료 관련 염증을 구별하기 어렵기 때문입니다." 펜실베이니아 대학교 페렐먼 의대의 신경 과학 교수이자 이 논문의 공동 수석 저자인 홍준 송 박사가 말했습니다. "이러한 오르가노이드는 개인의 뇌에서 일어나는 일을 매우 정확하게 반영하며, 앞으로 각 환자의 명백히 복잡한 종양을 '이해'하고 개인화된 의학에 가장 효과적인 치료법을 신속하게 결정하는 데 사용될 수 있기를 바랍니다."
CAR-T 세포 치료라고 불리는 한 가지 치료 방법은 환자 유래 T 세포를 재프로그래밍하여 신체의 특정 유형의 암 세포를 찾아 파괴하는 것입니다 . 이 치료법은 이미 미국 식품의약국(FDA)에서 여러 혈액암과 싸우도록 승인되었지만, 과학자들은 GBM과 같은 고형 종양을 성공적으로 찾아내어 사멸시키도록 면역 세포를 조작하는 데 어려움을 겪었습니다. 최근 연구에 따르면, 하나가 아닌 두 개의 뇌종양 관련 단백질을 표적으로 하는 CAR-T 세포 치료법이 재발성 GBM 환자의 고형 종양 성장을 줄이는 데 유망한 전략이 될 수 있다고 합니다.
"GBM을 치료하기 어려운 이유 중 하나는 종양이 매우 복잡하여 여러 유형의 암세포, 면역 세포, 혈관 및 기타 조직으로 구성되어 있기 때문입니다."라고 펜실베이니아 대학교 페렐먼 의대의 신경 과학 교수이자 공동 수석 저자인 Guo-li Ming 박사가 말했습니다. "단 하나의 유형의 암세포가 아닌 환자의 실제 종양의 작은 부분에서 오르가노이드를 성장시킴으로써 종양이 환자에게 존재하는 방식과 종양이 자라는 '미세 환경'을 반영할 수 있습니다. 이는 다른 기존 GBM 모델에는 반영되지 않습니다."
4.Cell Reports Medicine:Miltefosine reinvigorates exhausted T cells by targeting their bioenergetic state
T 세포 고갈을 극복하기 위해 다양한 전략이 제안되었는데, 여기에는 T 세포 고갈에 관련된 유전자 조작이 포함됩니다. TOX, NR4A, BATF, SNX9, CBLB, TGFBR2, ARID1A, REGNASE-1, 그리고 ROQUIN-1은 T 세포 고갈을 유도하는 것으로 보고되었습니다. 이들 유전자를 제거하면 T세포 기능이 향상될 수 있다. 또한, c-JUN, LTBR, IL-7 또는 CCL19는 CAR-T 세포 고갈을 완화하는 것으로 나타났으며, 여러 연구에서 이를 과발현하면 종양 제거가 향상될 수 있습니다. 그러나 CAR-T 치료의 고형 종양 치료에 대한 임상 효능은 여전히 제한적입니다. 게다가 ICB가 암 환자를 치료하는 데 있어 놀라운 임상적 성공을 거두었음에도 불구하고, 일부 환자만이 치료 후 완치에 도달합니다. 따라서 현재 치료법의 한계를 극복할 수 있는 효과적인 표적과 약물을 발견하는 것이 매우 바람직합니다.
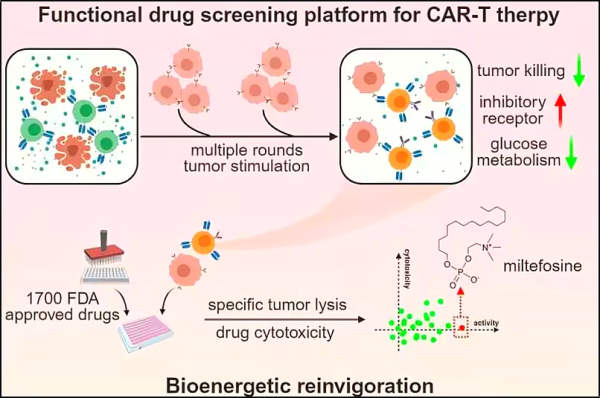
중국과학원, 중국과학원 대학, 베이징중의약대학, 베이징 줄기세포 및 재생의학 연구소, 인민해방군 일반병원, 선전대학의 연구진이 참여한 새로운 연구에서는 일차 인간 T세포를 사용하여 고갈된 T세포를 회복시키고 효능을 강화할 수 있는 화합물을 찾아내는 기능적 스크리닝 플랫폼을 개발했습니다. 관련 연구 결과는 2024년 12월 17일 "밀테포신은 생체 에너지 상태를 표적으로 삼아 지친 T 세포를 활력화합니다"라는 제목으로 저널 Cell Reports Medicine 에 게재되었습니다.
저자들은 이 플랫폼을 사용하여 미국 식품의약국(FDA) 승인 약물을 검토하고, 이전에 리슈마니아증에 대한 기생충 치료제로 사용된 소분자 밀테포신이 고갈된 CAR-T 세포의 효능을 높일 수 있다는 것을 발견했습니다.
PD-1/PD-L1 차단이 고갈된 T 세포의 효능을 향상시키는 메커니즘이자 성공적인 전략이라는 점을 감안하여, 저자들은 기능이 손상된 CAR-T 세포에 대한 밀테포신의 효과가 PD-1/PD-L1 경로에 따라 달라지는지 여부를 시험했습니다. 이를 시험하기 위해 그들은 PDCD1 유전자(PD-1을 인코딩)가 제거된 CAR-T 세포를 만들었고, 밀테포신이 여전히 그 효과기 기능을 향상시킬 수 있다는 것을 발견했습니다. 예상대로, 항 PD-1 항체는 PD-1 발현이 부족해 CAR-T 세포의 효과기 기능을 향상시키지 못했습니다.
5. Cell:YTHDF2 promotes ATP synthesis and immune evasion in B cell malignancies
키메라 항원 수용체(CAR)-T 세포 면역 요법 후 B세포 악성 종양 환자의 장기적이고 지속적인 완화는 종종 환자 신체에서 항원이 빠져나가기 때문에 여전히 만족스럽지 않습니다. 악성 B세포 변형과 종양 성장은 효율적인 ATP 합성에 의존하지만, 그 기저 메커니즘은 불분명합니다.
최근 국제 저널 Cell 에 게재된 "YTHDF2는 B 세포 악성 종양에서 ATP 합성과 면역 회피를 촉진한다" 라는 제목의 연구 보고서에서 City of Hope의 Beckman Research Institute와 다른 기관의 과학자들은 암 세포가 CAR-T 세포 치료를 회피하는 데 도움이 되는 핵심 원인을 발견했습니다. CAR-T 세포 치료는 숙주의 면역 체계를 사용하여 종양 세포를 찾아 죽일 수 있습니다. 이 치료법은 일반적으로 특정 유형의 백혈병과 림프종(예: 혈액암)에 사용됩니다. 그러나 일부 교활한 암 세포는 파괴되는 것을 피하기 위해 숙주의 면역 체계를 회피하는 방법을 배웠습니다. 관련 연구 결과는 암 환자의 생존을 개선하기 위한 보다 개인화된 치료법을 개발하는 데 도움이 될 것으로 기대됩니다.
이 논문에서 연구자들은 YTHDF2라는 특수 단백질이 혈액암 발생을 촉진하는 데 중요한 역할을 한다는 것을 발견했습니다. 그런 다음 그들은 YTHDF2 단백질을 표적으로 삼아 억제할 수 있는 새로운 약용 화합물 CCI-38을 개발했는데, 이는 공격적인 혈액암의 성장을 줄일 수 있습니다. 이 접근 방식은 암 치료의 성공 가능성을 높일 수 있습니다. Dr. Jianjun Chen은 "CCI-38을 사용하여 YTHDF2를 표적으로 삼는 것이 혈액암 세포에 대한 CAR-T 세포 치료의 효과를 크게 향상시킬 수 있다고 믿습니다."라고 말했습니다.
현재 혈액암 치료에 있어서 과제 중 하나는 '항원 탈출'이라고 불리는 현상이며, 이러한 치료법의 핵심 표적은 암세포에서 발견되는 CD19라는 단백질입니다. 그러나 28~68%의 경우 암세포가 CD19 마커를 감소시키거나 잃어버려 치료 효과가 떨어지며, 연구자들은 여러 성분을 표적으로 삼을 수 있는 전략을 조사하고 있지만 거의 절반의 환자는 여전히 이 문제로 영향을 받습니다. YTHDF2는 암세포가 꾸준한 에너지원을 생성하는 데 도움이 되는 유전자의 발현을 켜서 세포의 성장과 확산 능력을 촉진합니다. 또한, 이 단백질은 일반적으로 면역 체계가 암을 감지하고 공격하도록 하는 항원성 바이오마커의 존재를 줄임으로써 암세포가 스스로를 숨기도록 돕습니다. 마지막으로, 마우스 연구에서 과도한 YTHDF2는 늑대인간의 물림처럼 작용하여 혈액 세포를 건강한 상태에서 암 상태로 전환할 수 있습니다.
연구자들은 후속 치료의 필요성을 줄이는 것이 환자의 장기적 생존율을 높이고 질병 재발을 줄이는 동시에 치료의 부작용과 의료비도 줄일 수 있다고 지적합니다. YTHDF2 기능의 생물학적 기초를 밝히면 연구자들이 종양 세포가 면역 감시를 회피하는 것을 방지하는 새로운 전략을 개발하는 데 도움이 될 수 있으며, 이는 초기 치료에 반응하지 않거나 T 세포 기반 면역 요법에 대한 초기 반응 후 재발한 혈액암 환자를 치료하는 새로운 개인화 치료법을 개발하는 데 도움이 될 수 있습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.