2022년 CRISPR-Cas9을 이용해 유전자 특이적 표적 CAR-T 세포
페이지 정보
작성자 PnH 조회101회 작성일 24-05-17 14:22본문
특이적 표적 CAR-T 세포를 개발했으며 임상 시험에서 재발성/불응성 B 세포 비호지킨 림프종을 안전하고 효과적으로 치료할 수 있음을 확인했습니다.
최근 몇 년 동안 키메라항원수용체(CAR) T세포( CAR-T ) 치료법이 급속도로 발전해 암 치료에 큰 잠재력을 보였습니다. 그러나 현재 CAR-T 세포 치료제의 복잡한 제조 공정, 높은 생산 비용, 긴 준비 시간 및 잠재적인 안전성 문제를 포함하여 몇 가지 제한 사항이 여전히 존재합니다. CAR-T 세포 생산에 바이러스를 사용하는 것은 연구 분야인데, 이 접근법의 단점은 삽입된 돌연변이로 인한 종양 발생 위험 증가를 포함하기 때문입니다. 또한 바이러스 DNA에 대한 특정 반응은 종종 CAR 발현을 방해하고 바이러스 준비 자체는 비용이 많이 듭니다. 최근 여러 연구에서 게놈 편집 기술을 적용하여 아데노 관련 바이러스(AAV) 벡터를 템플릿으로 사용하여 유전자 특이적 통합된 CAR-T 세포를 생성할 수 있음이 입증되었습니다. 또한 돌연변이를 수정하고 T 세포 수용체(TCR)를 정확하게 삽입하는 T 세포를 이용하고 있습니다.

바이러스 사용과 무작위 통합의 단점을 동시에 해결하기 위해 중국 절강대학교, 화동사범대학교 등 연구기관 연구진이 CRISPR-Cas9을 이용해 유전자 특이적 표적 CAR-T 세포 개발 , 재발성/불응성 B 세포 비호지킨 림프종(r/r B-NHL) 환자 8명의 치료에서 1상에 높은 안전성이 공개 단일 임상 시험 성별 및 유효성 에서 관련 연구 결과는 최근 네이처(Nature) 저널에 "Non-viral, specifically targeted CAR-T cells achieve high safety and efficacy in B-NHL"라는 제목으로 게재되었습니다.
이들 저자에 따르면 임상 시험에서 유전자 특이적 표적 CAR-T 세포의 안전성과 효능을 세계 최초로 입증했습니다. CD19 표적 CAR을 PD1 유전자(PD1-19bbz CAR-T 세포)에 통합하는 CAR-T 세포를 사용함으로써, 그들은 이 CAR-T 세포로 치료받은 r/r B-NHL 환자가 놀라운 안전성을 갖는다는 것을 발견했습니다. 경미한 사이토카인 방출 증후군(CRS)의 발생률은 낮고 신경학적 독성은 발생하지 않는 장점 입니다. 그들의 전임상 실험은 또한 종양 세포가 PD-L1을 고도로 발현하는지 여부에 관계없이 PD1-19bbz CAR-T 세포가 이를 효율적으로 제거할 수 있음 을 보여주었습니다. 이러한 발견은 이전에 보고된 두 건의 임상 시험과도 일치하여 T 세포 요법에서 CRISPR-Cas9의 안전성을 추가로 확인합니다. 동시에 그들은 높은 완전 관해율과 지속적인 완전 관해를 관찰했습니다. 특히 PD-L1 발현이 높은 두 명의 r/r B-NHL 환자에서 반응이 발견되었습니다(한 명의 환자가 나중에 CD19-종양 재발을 일으켰지만). 놀랍게도, PD1-19bbz CAR-T 세포의 예상외로 낮은 초기 용량(체중 킬로그램당 2×106 세포 주입 ) 또는 CAR+ 세포의 생성을 야기하는 초기 및 아직 미흡한 제조 공정에도 불구하고 비율은 낮았습니다. 8명의 환자 중 7명은 12개월의 중간 관찰 기간 동안 완전한 관해를 달성했으며, 이는 이러한 PD1-19bbz CAR-T 세포가 종양 세포를 죽이는 더 강력한 효능을 가지고 있음을 시사합니다.
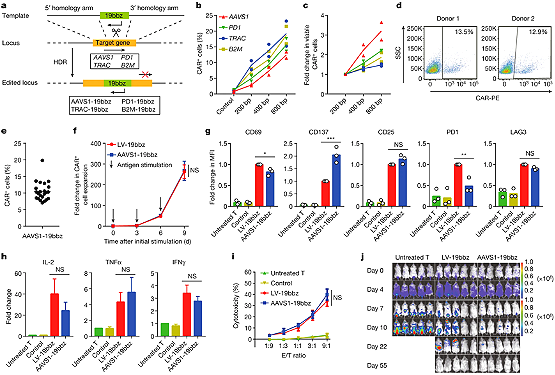
이미지: Nature, 2022, doi:10.1038/s41586-022-05140-y.
CAR을 AAVS1 유전자에 통합한 비바이러스성 CAR-T 세포는 종양 세포를 효과적으로 제거했습니다.
이들 저자의 전임상 및 임상 데이터는 PD1-19bbz CAR-T 세포가 종양 세포에 대해 더 높은 살상 효과를 갖는 것으로 나타났으며, 이는 두 가지 특징으로 설명될 수 있습니다.
첫째, 단세포 RNA 시퀀싱(scRNA-seq) 데이터는 PD1-19bbz CAR-T 세포 중 기억 T 세포의 높은 비율을 나타냈다.
둘째, 유전자 농축 분석 결과는 PD1 유전자에 CD19-표적 CAR을 통합함으로써 달성된 PD1의 파괴가 향상된 항종양 기능을 가진 PD1-19bbz CAR-T 세포를 부여했음을 보여주었습니다.
이러한 이점은 PD1-19bbz CAR-T 세포가 AAVS1 유전자에 CD19 표적 CAR을 통합한 CAR-T 세포와 비교하여 종양 세포를 더 강력하게 제거한다는 사실을 발견함으로써 실험 모델에서 확인되었습니다. 특히, 이러한 이점은 PD-L1 발현이 낮은 종양 세포에서도 관찰되었습니다. 또한 PD1 이외의 LAG3, TIM3 및 TIGIT와 같은 다른 억제 수용체가 임상 주입 후 PD1-19bbz CAR-T 세포에서 여전히 높게 발현된다는 점을 감안할 때 다중 억제 경로의 동시 개입은 CAR-T의 기능을 더욱 향상시킬 것으로 예상됩니다.
종합하면, 이 저자들은 CRISPR-Cas9를 통해 CAR-T 세포의 유전자 특이적 표적 개발을 위한 새로운 전략을 설명합니다. 이 기술은 제조 공정과 정확한 게놈 편집의 장점을 결합하기 때문에 발전합니다. 바이러스를 사용하지 않는 투인원(Two-in-One) 방식으로 CAR-T 세포 제조공정 간소화, 준비시간 단축, 생산원가 절감, CAR-T 세포 제품의 안전성과 유효성 향상 . 이러한 이점은 바이러스 준비 및 게놈 편집 프로세스를 동시에 수행해야 하는 경우가 많은 유전자 변형 CAR-T 세포의 제조에 특히 중요합니다. 또한, 위치별 통합은 CAR-T 세포의 동질성을 향상시켜 다기능 세포 제품을 활용할 수 있게 합니다. 중요한 것은 실험실에서 임상에 이르기까지 이 기술의 실현 가능한 적용을 시연했으며 임상 시험에서 높은 안전성과 효능을 입증했다는 것입니다. 따라서 기존의 장벽을 뛰어넘는 혁신적인 CAR-T 세포 기술을 제안했고, CRISPR-Cas9 매개 유전자 특이적 표적 기술의 세포치료제 잠재력을 입증했습니다.
참고문헌입니다
Jiqin Zhang et al. Non-viral, specifically targeted CAR-T cells achieve high safety and efficacy in B-NHL. Nature, 2022, doi:10.1038/s41586-022-05140-y.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.










