2025년 Nature Communications:CRISPR/Cas9 editing of NKG2A improves the efficacy of primary CD33-directed chimeric antigen receptor natural killer cells
페이지 정보
작성자 PnH 조회26회 작성일 25-02-07 17:10본문
이번 연구 결과는 NKG2A가 결핍된 CAR-NK 세포가 환자의 급성 골수성 백혈병으로 인한 면역 억제 효과를 우회할 수 있음을 보여줍니다.
현재 인간에게는 많은 형태의 혈액암이 있으며, 이를 통틀어 백혈병 이라고 합니다. 급성 골수성 백혈병(AML)은 흔한 백혈병의 한 형태입니다. 주요 특징은 환자의 초기 혈액 세포 전구체(즉, 줄기 세포 와 줄기 세포에서 발달한 전구 세포) 가 분해되는 것입니다 . 이 유형의 백혈병 환자는 집중적인 화학 요법을 받지만, 진단 및 치료 후 5년을 살아남는 사람은 20%-50%에 불과합니다. 이들의 상태를 복잡하게 만드는 것은 이러한 집중적인 요법이 신체의 조혈 줄기 세포 에 파괴적인 영향을 미치며 , 이는 종종 더 심각한 부작용과 관련이 있다는 사실입니다. 이것이 연구자들이 새로운 치료법을 개발해야 하는 절실한 이유입니다.
최근 국제 학술지 Nature Communications 에 게재된 "CRISPR/Cas9 editing of NKG2A improvements the efficiency of primary CD33-directed chimeric antigen receptor natural killer cells" 라는 제목의 연구 보고서에서 , 프랑크푸르트 괴테 대학과 다른 기관의 과학자들은 연구를 통해 CAR-NK 세포를 성공적으로 변형시켰으며, 이는 인간 백혈병과 싸우는 또 다른 대체 방법으로 사용될 가능성이 있습니다. 연구자들은 면역 요법이 숙주의 면역 체계의 자연적인 힘을 이용해 악성 백혈병 세포와 싸울 수 있다고 설명했습니다. 이 요법의 일환으로 암세포는 T세포와 같은 신체 면역 체계의 킬러 세포에 의해 인식될 수 있습니다. 예를 들어, T세포 표면에는 자물쇠와 같은 구조가 있으며, 암세포 표면에 있는 해당 구조를 열쇠처럼 삽입할 수 있습니다. 기술적인 관점에서 T세포의 자물쇠를 "항원 수용체"라고 하고 열쇠를 "항원"이라고 합니다.
열쇠가 자물쇠에 있다면, 즉 항원과 항체가 결합하면 T 세포가 세포를 죽일 것입니다. 이제 연구자들은 항원 수용체를 사용자 정의하여 특정 종양 특징을 인식할 수 있습니다. 이를 위해 연구자들은 환자의 혈액에서 T 세포를 추출하고 유전공학을 사용하여 소위 키메라 항원 수용체(CAR)를 삽입했습니다. 이는 여러 단백질의 특성을 결합하여 세포가 특별한 방식으로 질병을 표적으로 삼을 수 있도록 합니다. 공격은 특정 종양에 최적화되었습니다. . 키메라 항원 수용체( CAR-T 세포)를 갖춘 T 세포는 인간 백혈병을 치료하는 데 성공적으로 사용되었으며 현재 사용 중인 또 다른 유형의 킬러 세포는 소위 자연 킬러 세포(NK 세포)입니다. 악성 세포를 인식하는 대신 특정 항원에 대해서는 다른 표면 이상에 의존합니다. 키메라 항원 수용체를 추가하면 두 가지 방법으로 암세포와 싸울 수 있습니다. 한 가지 장점은 지금까지 임상 연구에서 부작용이 거의 발생하지 않았다는 것입니다.
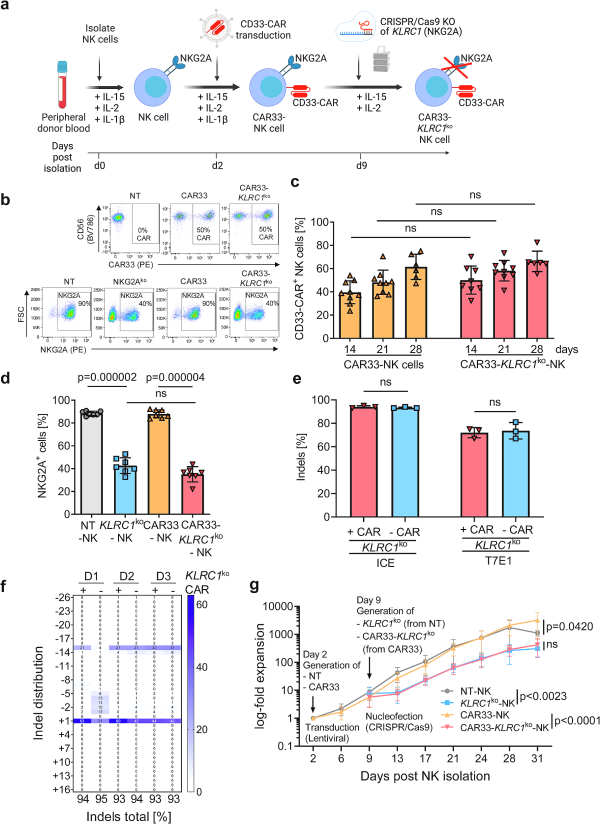
CAR33-KLRC1 KO -NK 세포 에서 CRISPR/Cas9 녹아웃의 생성 및 평가
그러나 암세포는 이러한 면역 세포의 공격을 회피하는 여러 가지 방법을 가지고 있는데, 여기에는 공격 전에 면역 세포의 기능을 단순히 중단하는 것도 포함됩니다. 이를 위해 그들은 면역 세포 표면의 단백질로 구성된 특수 체크포인트에 의존합니다. 이 면역 체크포인트는 항원 수용체에 결합하는 모든 세포를 특별히 체크하여 신체의 세포 중 하나가 아닌지 확인합니다. 신체의 세포가 결합한 경우 체크포인트에 해당 반응이 나타나 면역 공격을 중단시킵니다. 건강한 신체에서는 이 과정이 면역 세포가 부주의로 신체의 정상 세포를 공격하여 심각한 손상을 입히는 것을 방지합니다.
암세포는 원래 신체 자체의 세포이고, 일부는 체크포인트와 통신하여 면역 세포 공격을 차단할 수 있기 때문에 이러한 공격은 CAR 면역 세포에도 영향을 미칠 수 있으며, 이는 현재 면역 요법에 큰 문제를 일으킵니다. 이것이 면역 요법이 종종 약물과 결합되는 이유입니다. 면역 세포 검문소를 보호하여 암세포가 더 이상 이 검문소에 침입할 수 없도록 합니다. 이 연구에서 울리히의 팀은 맞춤형 면역 세포 기능이 중단되는 것을 방지하는 또 다른 방법을 발견했습니다. 실험실 실험에서 그들은 NK 세포의 중요한 면역 체크포인트를 성공적으로 완전히 중단했습니다. 특히 AML 세포를 표적으로 삼습니다. 이를 위해 연구진은 CRISPR/Cas 유전자 편집 기술을 사용하여 체크포인트 형성을 막는 방식으로 해당 유전자를 차단했고, 이를 통해 암세포가 환자 신체에서 면역 관용을 일으키는 것을 성공적으로 예방했습니다.
연구자들은 면역 체크포인트가 없는 CAR-NK 세포가 CAR 수용체를 가지고 있거나 면역 체크포인트가 없는 NK 세포보다 AML 환자의 암 세포를 더 효과적으로 죽일 수 있다고 말했습니다. 연구원 Bexte는 암 세포와 싸우기 위해 우리의 이중 Modifying NK 세포가 유망할 수도 있다고 설명했습니다. 암세포의 분자적 특징은 종종 치료에 대한 저항성 증가와 관련이 있습니다. 그런 다음 연구진은 연구를 위해 인간 AML 세포를 쥐에 이식했고, 이중 변형 NK 세포를 투여했을 때 약물 복용량을 상당히 줄였음에도 불구하고 쥐가 훨씬 더 오래 생존한다는 것을 발견했습니다.
연구자들은 향후 연구에서 이러한 맞춤형 면역 세포가 인체에서도 역할을 할 수 있는지 확인하기 위해 보다 심층적인 연구를 수행하기를 바라고 있습니다. 요약하면, 이 연구 결과는 NKG2A가 결핍된 CAR-NK 세포가 환자의 급성 골수성 백혈병의 면역 억제 효과를 우회할 수 있음을 보여줍니다.
Bexte, T., Albinger, N., Al Ajami, A. et al. CRISPR/Cas9 editing of NKG2A improves the efficacy of primary CD33-directed chimeric antigen receptor natural killer cells. Nat Commun 15, 8439 (2024). doi:10.1038/s41467-024-52388-1
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.