2023년 : CAR-T 연구 발표 최신 논문
페이지 정보
작성자 PnH 조회88회 작성일 24-05-31 03:22본문
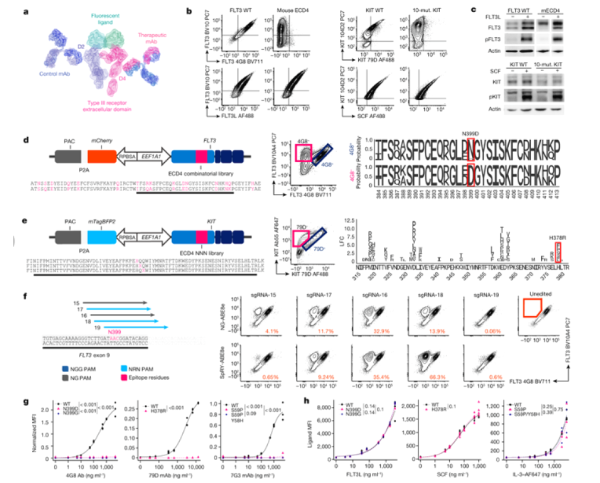
[1] Nature: Epitope 편집 기술을 통해 CAR-T 세포 및 단일클론항체 치료법의 효능을 향상시킬 것으로 기대
불필요한 계통 항원(예: B세포 급성 림프구성 백혈병의 CD19 ) 유전자는 조혈 줄기 /전구세포(HSPC) 또는 분화된 골수세포에서 발현되어 환자에게 견딜 수 없는 표적 질병을 일으키거나 표적을 벗어난 종양 독성 효과를 초래합니다.
최근 국제학술지 네이처 (Nature) 에 게재 된 "Epitope editing enables targeted immunotherapy of acute myeloid leukaemia"라는 연구 보고서에서 다나-파버 암 연구소(Dana-Farber Cancer Institute) 등의 과학자들은 기증자 조혈줄기/전구세포 개발을 위한 연구를 진행했습니다.
Nature (2023) DOI:10.1038/s41586-023-06496-5
숙주의 면역 체계가 외부 항원(병원체 또는 종양의 일부)을 만나면 이를 인식하고 중화하려고 시도합니다. Epitope는 면역 체계가 보고 중화할 수 있는 이러한 항원의 일부이며, Epitope를 유발하는 특별한 표적으로 간주됩니다. 키메라 항원 수용체(CAR) T 세포와 단클론 항체는 "불량 세포"의 항원을 표적으로 삼아 혈액 악성 종양을 치료하는 데 큰 가능성을 보였지만, 종양 특이적 표지가 부족하여 AML에서의 사용이 제한되어 왔습니다. 치료 중에 숙주의 건강한 세포와 조직이 손상될 위험이 있습니다.
특히 골수 이식을 위해 기증 유기체로부터 얻은 조혈 줄기/Epitope 세포의 편집이 이러한 문제에 대한 가능한 해결책이 될 수 있습니다. HSPC에서 FLT3, CD123 및 KIT와 같은 특정 유전자의 변형은 Epitope 마커를 변경할 수 있지만 유전자의 정상적인 기능을 변경하지는 않습니다. 이 접근법은 암세포를 보다 효과적으로 표적으로 삼는 동시에 건강한 세포를 보호하고 유해한 표적 외 부작용을 줄임으로써 치료법의 안전성과 효과를 향상시킬 수 있습니다.
[2] Stem Cell Reports: DOX, doxorubicin의 기술로 항암치료의 표적화를 확인하였습니다.
화학요법은 암환자의 주요 치료법 중 하나로, 화학요법 약물은 체내 암세포를 파괴할 수 있지만, 약물이 암세포를 선택적으로 죽이지 못하고 건강한 세포에 독성 영향을 미치기 때문에 암환자는 종종 다양한 상황에 직면하게 됩니다.
최근 국제학술지 Stem Cell Reports 에 게재된 "Protein-Encapsulated Doxorubicin Reduces Cardiotoxicity in hiPSC-Cardiomyocytes and Cardiac Spheroids While Maintaining Anticancer Efficacy"라는 제목의 연구 보고서에서 Cedars-Sinai Medical Center 및 기타 기관의 과학자들이 연구를 통해 단일 단백질 캡슐화 DOX(SPEDOX-6, 단일 단백질 캡슐화 DOX)를 사용하여 표적 암 치료법을 제공하고 신체의 심장 세포 건강을 보호할 것으로 예상됩니다.
연구자들은 (DOX, doxorubicin)이 유방암이나 특정 유형의 혈액암 환자를 치료하는 데 자주 사용되는 특수 화학요법 약물이라고 말하지만, 현재 이를 투여받는 환자의 최대 1/3은 고용량으로 치료받는 환자들입니다. DOX, doxorubicin은
장기적으로 심부전으로 이어질 수 있는 심장 손상을 경험합니다. 암세포와 마찬가지로 DOX, doxorubicin도 정상적인 심장 세포에 침투하여 DNA를 손상시키고 궁극적으로 세포 사멸을 일으킬 수 있습니다.
암세포에 대한 DOX, doxorubicin의 특이성을 높이기 위해 연구자들은 DOX, doxorubicin을 캡슐화하기 위해 단백질 껍질을 사용하는 새로운 방법을 개발했습니다. SPEDOX-6이라고 불리는 이 새로운 공식/새로운 방법은 빠르게 분열하는 세포(예: 암)에 대한 약물 전달을 증가시킬 수 있습니다. 인간 암세포에서 유래한 심장세포와 인간 줄기세포를 실험실에서 분석한 결과, 연구진은 DOX, doxorubicin과 마찬가지로 암에 대한 독성이 더 강한 것으로 확인했습니다.
전통적인 DOX, doxorubicin보다 정상적인 심장 세포에 독성이 적습니다.
[3] Molecular Cancer Research: 에스트로겐 수용체 돌연변이에 대한 연구는 자궁내막암에 대한 새로운 맞춤형 치료법 개발에 도움이 될 수 있습니다.
활성화 에스트로겐 수용체 알파(ER, ESR1로도 알려져 있음) 돌연변이는 원발성 자궁내막암과 전이성 유방암에 존재하여 유방암의 기능적 특징인 에스트로겐 비의존성 수용체 활성화를 촉진합니다. 이 수용체의 독특한 분자 및 표현형 결과가 확인되었습니다 그러나 ER 돌연변이가 자궁내막암에 미치는 영향은 아직까지 해명되지 않았으며,
최근 국제학술지 Molecular Cancer Research에 ' Allele-specific Gene Regulation, Phenotypes, and Therapeutic Vulnerabilities in Estrogen Receptor Alpha–mutant Endometrial Cancer'이라는 제목의 논문이 게재됐습니다. – 돌연변이 자궁내막암'이라는 연구를 통해 유타대학교 및 기타 기관 연구원들이 연구를 통해 자궁내막암 환자에게 새로운 치료 옵션을 제시할 것으로 기대됩니다.
자궁내막암은 가장 흔한 부인과암 중 하나이며, 높은 수준의 에스트로겐이 그 진행을 촉진하는데, 연구진은 자궁내막암에서 발견되는 에스트로겐 수용체 돌연변이가 자궁내막암 발병 위험을 증가시키고 세포에 큰 변화를 일으킨다는 사실을 발견했습니다. 에스트로겐은 에스트로겐 수용체에 결합하여 이를 활성화시키는 생식 호르몬입니다. 암은 또한 에스트로겐 수용체를 활성 상태로 유지시켜 자궁내막의 종양을 증가시킬 수 있습니다. "우리의 목표는 자궁내막암에서 에스트로겐 수용체 돌연변이를 특성화하고 그것이 유전자 발현에 어떤 영향을 미치는지, 그리고 이러한 돌연변이가 어떻게 세포를 더 빠르게 성장하게 하는지를 확인하는 것이었습니다."라고 Zannel Blanchard 박사는 말했습니다. 돌연변이는 유전자 발현과 세포 행동에 극적인 변화를 가져올 수 있습니다.
연구진은 연구 결과를 바탕으로 에스트로겐 수용체 활성도가 높은 자궁내막암 환자를 치료하는 방법을 확인했으며, 에스트로겐 수용체와 시너지 효과를 발휘하는 CDK9 단백질 억제제가 자궁내막암 위험을 줄이는 데 효과적일 수 있다는 사실을 발견했습니다.
【4】Cell Metabolism: 일반적인 항응고제인 와파린이 새로운 암 치료법으로 방향 전환될 수 있습니다
최근 국제잡지 Cell Metabolism 에 게재 된 "Regulation of VKORC1L1 is critical for p53-mediated tumor suppression through vitamin K metabolism"라는 제목의 연구 보고서에서 컬럼비아 대학 및 기타 기관의 연구원들은 연구를 통해 광범위한 혈액 희석제 와파린이 나타나는 것을 발견했습니다. 세포와 동물실험에 대한 연구를 통해 연구자들은 와파린이 종양 개입 세포가 돌연변이나 기타 이상을 감지하는 것을 방지한다고 확인했습니다.
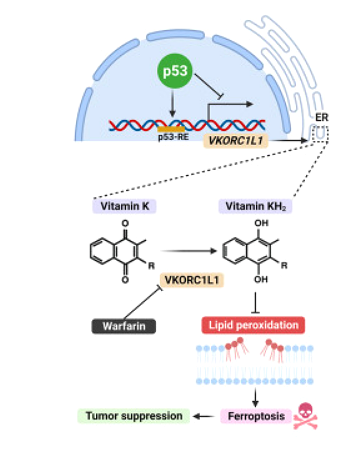
(2023) DOI:10.1016/j.cmet.2023.06.014
Wei Gu 연구원은 이 연구 결과에 따르면 현재 FDA에서 사용하도록 승인된 와파린이 췌장암을 포함한 다양한 암 치료에 용도가 변경될 수 있음을 나타냅니다. 와파린의 발견은 최근 발견된 암의 세포 사멸 메커니즘인 페롭토시스(ferroptosis)를 조절하는 분자적 과정을 규명하기 위한 연구에서 의외의 결과였습니다. 기능을 수행하려면 철분이 필요하며, 페롭토시스를 유발하는 약물은 현재 치료할 수 없는 암 유형에 특히 유용합니다.
세포 내에서 페로프토시스가 조절되는 메커니즘 에 대해 더 자세히 알아보기 위해 연구자들은 페로프토시스를 촉진하는 유전자를 확인하기 위해 인간 흑색종 세포에 대한 유전적 스크리닝을 실시했습니다. 예상대로 연구자들은 이전에 알려진 여러 페로프토시스 유전자에 추가로 스크리닝을 실시했습니다. VKORC1L1이라는 유전자도 발견됐습니다.
연구자들은 VKORC1L1이 페롭토시스의 잠재적 억제제이며, VKORC1L1의 상실로 인해 세포가 페롭토시스 세포 사멸에 민감해진다는 사실을 발견했습니다. 암 데이터 분석에 따르면 VKORC1L1 수준에는 임상적 결과도 있음이 시사됩니다. 즉, VKORC1L1 활성 수준이 낮은 환자는 일반적으로 VKORC1L1 수준이 높은 환자보다 더 오래 삽니다.
【5】 Science Translational Medicine: 역형성 대세포 림프종 치료를 위한 새로운 병용요법 개발 기대
역형성 대세포 림프종은 비호지킨 림프종의 일종으로 소아에서 가장 흔한 공격성 림프종으로 화학요법과 방사선 요법으로 약 30%의 사례는 치료할 수 없습니다. 대부분의 소아에서 크리조티닙과 같은 키나제 억제제 약물은 화학요법의 심각한 부작용을 일으키지 않으면서 종양 성장을 효과적으로 차단할 수 있습니다.
그러나 ALK 억제제는 매우 비싸고(환자의 연간 비용 약 $80,000) 평생 복용해야 합니다. 환자가 중단하면 림프종이 재발합니다. 연구자들은 ALK 억제제가 림프종을 조절할 수 있지만 치료할 수는 없다는 것을 알고 있습니다.
(Science Translational Medicine) 에 게재 된 "Targeting CCR7-PI3Kγ overcomes resistance to tyrosine kinase inhibitors in ALK-rearranged lymphom"라는 제목의 연구 보고서에서 이탈리아 토리노 대학 및 기타 기관의 연구자들이 연구를 통해 도움을 줄 것으로 기대됩니다. 역형성 대세포 림프종 치료를 위한 새로운 치료법을 개발합니다. 기사에서 연구자들은 재발성 역형성 대세포 림프종 환자를 대상으로 새로운 병용 요법의 효과를 테스트하는 프로그램을 시작했습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.