2023년 10월 CAR-T연구 면역세포치료 요약
페이지 정보
작성자 PnH 조회97회 작성일 24-05-31 04:08본문
CAR-T (Chimeric Antigen Receptor T- Cell Immunotherapy), 즉 키메라 항원 수용체 T세포 면역치료법 . 이 치료법은 수년 동안 사용되어 왔지만 최근 몇 년간 임상적으로 개선되어 사용된 새로운 유형의 세포 치료법입니다. 급성 백혈병 과 비호지킨 림프종 치료에 상당한 효능이 있으며 가장 유망한 암 치료법 중 하나입니니다. 모든 기술과 마찬가지로 CAR-T 기술도 오랜 진화 과정을 거쳐 왔으며, 이러한 일련의 진화 과정을 거치면서 CAR-T 기술도 점차 했습니다.
이 새로운 치료의 핵심은 표적 세포를 인식하고 환자의 T세포가 CAR을 발현하도록 유전적으로 변형된 키메라 항원 수용체(CAR)라는 인공 수용체입니다. 임상 시험에서 연구원들은 투석과 유사한 과정을 통해 환자로부터 일부 T 세포를 추출한 다음 배양실에서 이를 유전적으로 변형하고 이 T 세포가 이 새로운 수용체를 발현할 수 있도록 이 CAR을 암호화하는 유전자를 도입했습니다. 이러한 유전적으로 변형된 T 세포는 실험실에서 증식된 다음 환자에게 다시 주입됩니다. 이러한 T 세포는 자신이 발현하는 CAR 수용체를 사용하여 표적 세포 표면의 분자에 결합하고, 이 결합은 내부 신호를 촉발하여 T 세포를 매우 강력하게 활성화시켜 표적 세포를 빠르게 파괴합니다.
최근에는 급성 백혈병과 비호지킨 림프종 치료에 사용되는 것 외에도 CAR-T 면역요법은 고형 종양, 자가면역 질환, HIV 감염, 심장 질환 및 기타 질병 치료에도 개선되어 적용 범위가 넓어졌습니다.
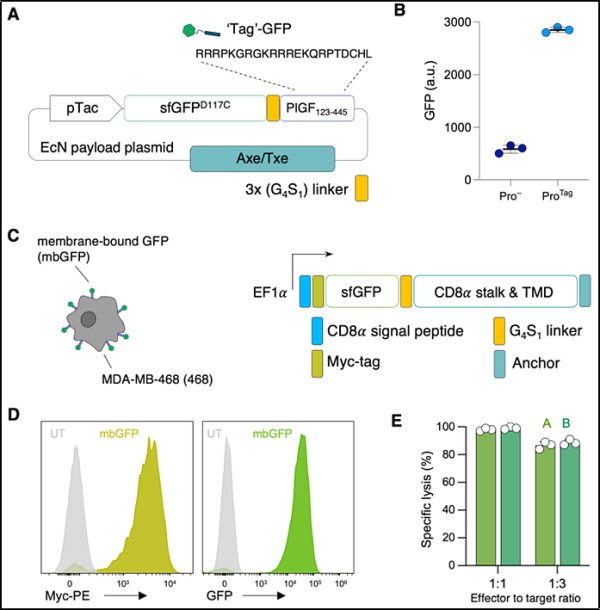
1. Science: Probiotic-guided CAR-T cells for solid tumor targeting
수년 동안 연구원들은 백혈병과 림프종 환자를 치료하기 위해 혈액 세포 표면의 특정 항원을 표적으로 삼는 키메라 항원 수용체(CAR) T 세포(CAR-T)를 성공적으로 사용해 왔습니다. 그러나 유방암 이나 대장암 과 같은 고형 종양을 표적으로 삼기 위해 CAR T 세포를 사용하는 것은 특히 어려운 것으로 입증되었습니다. 고형 종양에는 다양한 항원을 표시하는 다양한 세포가 포함되어 있으며 신체의 건강한 세포도 종종 이러한 항원을 발현합니다. 따라서 일관되고 안전한 종양 표적을 식별하는 것은 개발 첫 단계에서 고형 종양에 대한 대부분의 CAR-T 세포 치료법의 성공을 방해했습니다.
Science, 2023, doi:10.1126/science.add7034
논문의 교신저자이자 컬럼비아대학교 생의학공학 부교수인 탈 다니노(Tal Danino)는 "우리의 프로바이오틱스 플랫폼은 CAR-T 세포가 여러 유형의 종양을 공격할 수 있게 합니다. 전통적인 CAR-T 세포 치료법은 자연 종양 항원을 표적으로 삼는 데 의존합니다"고 말했습니다. 이는 유전자 변형 T 세포와 유전자 변형 박테리아를 결합하여 합성 항원을 고형 종양에 안전하고 체계적이며 효과적으로 전달하는 첫 번째 사례입니다. 이는 많은 암 치료에 큰 영향을 미칠 것입니다."
종양을 찾는 박테리아를 프로그래밍하고 CAR-T 세포가 인식할 수 있는 합성 항원으로 고형 종양을 코팅함으로써 Danino의 연구실은 본질적으로 보편적인 항원을 공격할 수 있는 보편적인 CAR-T 세포를 구축합니다. 이 프로바이오틱스 유도 CAR-T 세포(ProCAR) 플랫폼은 저자들이 유전자 변형 프로바이오틱스와 CAR-T 세포를 성공적으로 결합한 최초의 사례이며, CAR-T 세포가 직접 생산된 합성 항원에 반응한다는 사실을 입증한 최초의 사례이기도 합니다.
논문의 공동 제1저자이자 다니노 연구실의 박사과정 학생인 로사 빈센트(Rosa Vincent)는 “종양 표적 박테리아와 CAR-T 세포를 결합하는 이점은 새로운 종양 인식 전략을 제공하며 이는 유전자 변형 기술을 개발하는 새로운 방법을 제공한다”고 말했습니다. 생체 내 치료를 위한 박테리아 공동체가 기반을 마련했습니다. 우리는 이 두 가지 세포 치료의 가장 좋은 특징, 즉 박테리아를 사용하여 종양 표적을 생성하는 것과 T 세포를 사용하여 악성 종양 . 이 두 가지 유형의 세포 치료법 사이에는 각각의 치료법마다 고유한 한계가 있습니다."
2. Blood Advances: Racial and ethnic differences in clinical outcomes among multiple myeloma patients treated with CAR T-cell therapy
이데카바겐 비클루셀(ide-cel이라고도 함)이라는 키메라 항원 수용체(CAR) T세포(CAR-T) 치료법을 받은 다발성 골수종 환자가 인종과 민족에 관계없이 더 나은 결과를 보였다는 새로운 연구 결과가 나왔습니다. 두 그룹 사이의 전체 생존율에는 차이가 없었습니다.
관련 연구 결과는 'Racial and ethnic differences in clinical outcomes among multiple myeloma patients treated with CAR T-cell therapy'라는 제목으로 2023년 10월 16일자 Blood Advances 저널에 온라인 게재됐습니다.
Blood Advances, 2023, doi:10.1182/ bloodadvances.2023010894
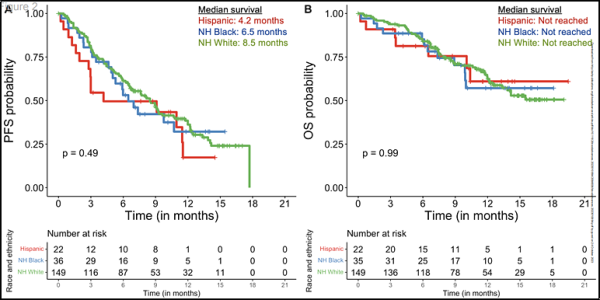
새로운 연구를 수행하기 위해 페레스 박사와 그녀의 연구팀은 미국 다발성 골수종 면역치료 컨소시엄에 참여하는 11개 기관의 207명의 환자로부터 데이터를 수집했습니다. 총 149명(72%)의 환자는 비히스패닉 백인, 30명(17%)은 비히스패닉 흑인, 22명(11%)은 히스패닉으로 확인되었습니다. 페레스 연구팀은 이데셀을 투여받은 재발성/불응성 다발골수종 환자를 대상으로 치료 후 약 9개월 동안 반응률, 전체 생존율, CAR-T 세포 관련 합병증 발생률을 모니터링한 뒤 추적 관찰했습니다.
이러한 연구 결과는 비히스패닉계 흑인 환자(97%)가 히스패닉계 백인 환자(77%) 및 비히스패닉계 백인 환자(85%)에 비해 염증을 유발하는 기저 질환인 사이토카인 방출 증후군이 발생할 가능성이 더 높다는 것을 나타 냅니다. . 그러나 페레스 팀은 다양한 인종과 민족의 환자들 사이에서 결과를 비교했을 때 심각한 합병증이 발생할 가능성에 큰 차이가 없음을 발견했습니다. 마찬가지로 중환자실 입원 발생률, 완전 관해 달성 가능성, 전체 생존율에서도 흑인과 백인 환자 사이에 유의미한 차이가 없음을 발견했습니다.
전체 반응률(즉, CAR-T에 대해 부분적, 매우 우수한 부분적 또는 완전 반응을 달성한 환자의 비율)은 비히스패닉계 흑인 및 백인 환자에 비해 히스패닉계 환자에서 더 낮았지만 연구자들은 이것이 부분적으로 연구에 참여하는 히스패닉계 환자 수가 제한되어 있기 때문입니다.
3.Polymers for Advanced Technologies: Synthesis of guanidinium-dendrimer-type pDNA carriers for gene delivery into floating blood cells
새로운 연구에서 일본 도쿄 메트로폴리탄 대학의 연구자들은 혈액암의 핵심 치료법인 키메라 항원 수용체(CAR) T세포(CAR-T) 치료에 사용할 수 있는 새로운 폴리머를 발견했습니다.플라스미드 DNA의 효율적인 전달 세포치료에서는 T세포로 전환됩니다. 중요한 것은 표면에 고정된 T 세포뿐만 아니라 떠다니는 T 세포에도 유전자를 전달한다는 것입니다. 안정적이고 독성이 없으며 바이러스를 사용하지 않습니다. 이는 현장에서 표준으로 간주되는 다중이온 화합물보다 성능이 뛰어나 새로운 치료법의 길을 열어줍니다. 관련 연구 결과는 최근 Polymers for Advanced Technologies 저널에 "Synthesis of guanidinium-dendrimer-type pDNA carriers for gene delivery into floating blood cells"이라는 제목으로 게재되었습니다.
2023, doi:10.1002/pat.6136의 이미지
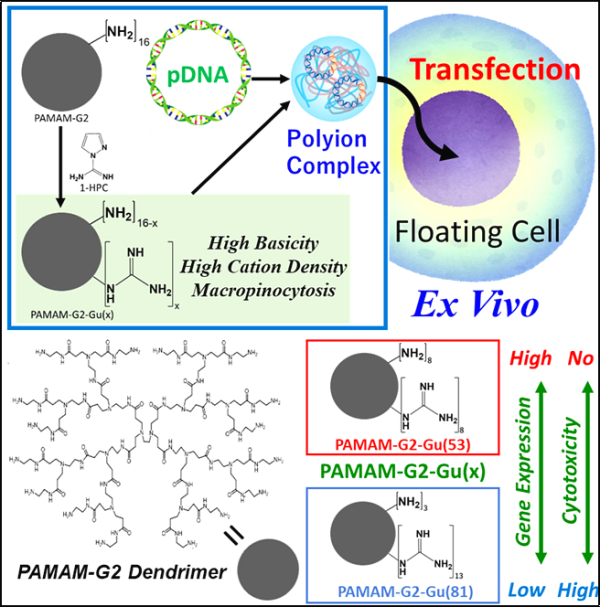
새로운 연구에서 도쿄 수도 대학의 아사야마 쇼이치로(Shoichiro Asayama) 교수가 이끄는 연구팀은 플라스미드 DNA를 떠다니는 T 세포에 효율적으로 전달할 수 있는 새로운 고분자 화합물을 구축했습니다. 그들은 헤어볼과 유사한 가지 모양의 구조를 가진 대형 폴리머인 덴드리머를 사용했습니다. 구체적으로 그들은 2세대 폴리아미도아민(PAMAM-G2)을 사용했는데, 여기서 2세대는 중앙 구조에서 바깥쪽으로 형성되는 새로운 가지의 수를 의미합니다. 이들 가지의 끝을 변형하는 실험에서 그들은 플라스미드 DNA와 PAMAM-G2 사이의 다양한 결합 행동이 달성될 수 있음을 발견했습니다.
특히, 이 저자들은 PAMAM-G2의 분지 말단에 있는 특정 비율의 1차 아민 그룹을 매우 염기성인 구아니딘(Gu) 그룹으로 대체함으로써 PAMAM-G2가 플라스미드 DNA에 대한 탁월한 운반체임을 발견했습니다. PAMAM-G2-Gu는 세포가 이물질을 "잡아먹는" 흡수하는 일반적인 메커니즘인 거대음작용(macropinocytosis)을 위해 고도로 전하되고 크기가 조정됩니다.
올바른 제제를 사용하면 새로운 고분자 화합물은 무독성이며 혈장에서도 안정적입니다. 가장 중요한 것은 플랑크톤 T 세포에 대한 테스트에서 PAMAM-G2-Gu(53)(구아니딘으로 대체된 53%)가 분지형 폴리에틸렌이민(bPEI)보다 훨씬 더 나은 성능을 발휘했다는 것입니다. bPEI는 유전자 형질감염의 최적 표준 PIC입니다.
낮은 독성과 우수한 벡터 특성을 고려할 때, 저자들은 다양한 생명을 위협하는 질병에 대한 차세대 CAR-T 세포 치료법에서 시험관 내 및 생체 내 형질감염을 위한 실행 가능한 후보를 찾았다고 믿습니다.
4.Int J Biol Sci:Enhanced tumor immunotherapy by polyfunctional CD19-CAR T cells engineered to secrete anti-CD47 single-chain variable fragment
최근 Southern Medical University의 연구진은 Int J Biol Sci 저널에 "Enhanced tumor immunotherapy by polyfunctional CD19-CAR T cells engineered to secrete anti-CD47 single-chain variable fragment"라는 제목의 논문을 게재했습니다. CAR T 세포에 의한 항-CD47은 전신 항체 치료와 관련된 독성을 제한할 수 있으므로, 이 연구는 강화된 종양 면역 치료를 위한 CAR T 세포 형질전환에 대한 보다 효과적이고 안전한 접근 방식을 제공합니다.
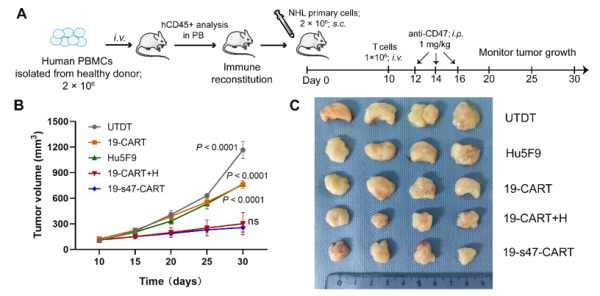
CD19-s47-CAR T 세포의 항종양 및 면역조절 효과
키메라 항원 수용체 T(CAR T) 세포 치료 후 비호지킨 림프종(NHL)의 높은 재발률은 여전히 병목 현상으로 남아 있으며, 면역억제성 종양 미세환경(TME)은 NHL에서 CAR T 세포의 효능을 손상시키는 재발의 주요 원인입니다. . 따라서 CAR T 세포의 구조를 변화시켜 TME의 억제 효과를 약화시켜 재발률을 낮추는 것은 귀중한 연구 주제입니다. CD47은 유망한 치료 표적인 것으로 나타났으며 대식세포 기능을 조절하는 데 중요합니다.
여기에서 연구자들은 CD19-CAR T 세포를 조작하여 항CD47 단일 사슬 가변 단편(scFv)을 분비하고 항종양 효능 강화, T 세포 분화 조절, 대식세포 식균 작용 및 분극화를 시험관 내 및 생체 내에서 변경하는 역할을 확인했습니다. 연구 화학적 기능. 효능은 CAR T 세포와 CD47 항체의 조합과 유사하거나 우수했습니다. 특히, 항-CD47 scFv를 분비하는 CAR T 세포는 모 CAR T 세포와 비교하여 더 효율적인 탈과립화 및 다기능성 사이토카인을 특징으로 하는 특정 항원 자극 시 더 강력한 면역 반응을 생성합니다. 또한 CAR T 세포에 의한 항-CD47의 국소 전달은 전신 항체 요법과 관련된 독성을 제한할 수 있습니다.
5. Neuro-Oncology: NLGN4X TCR transgenic T cells to treat gliomas.
교모세포종은 가장 공격적인 뇌종양이다. 이는 뇌에 광범위하게 퍼지며 수술로 완전히 제거하기가 어렵습니다. 화학요법이나 방사선 요법 역시 효과가 제한적인 경우가 많습니다. 환자를 위한 새롭고 보다 효과적인 치료법을 찾기 위해 의사와 과학자들은 소위 "선택된" T 세포 치료법을 포함하여 다양한 면역 치료법을 테스트하고 있습니다. 여기에는 환자의 신체에서 T 세포를 분리하여 배양 접시에서 성장시키는 것이 포함됩니다. 그들은 변형된 후 환자에게 다시 이식됩니다. 의사들은 다양한 접근법을 추구하고 있습니다.
새로운 연구에서 독일 암 연구 센터와 만하임 대학 의료 센터의 연구원들은 생쥐의 뇌종양에 대한 새로운 세포 기반 면역 치료법을 처음으로 성공적으로 테스트했습니다. 관련 연구 결과는 최근 Neuro-Oncology 저널에 "NLGN4X TCR transgenic T cells to treat gliomas"라는 제목으로 게재되었습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.