2023년 Science: 10월 발표 논문 (2)
페이지 정보
작성자 PnH 조회95회 작성일 24-05-31 04:01본문
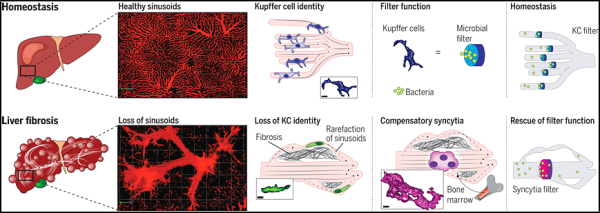
1. Science: 섬유화된 간에 대식세포기능을 하는 쿠퍼유사 세포를 확인하였습니다.
캐나다 캘거리 대학교와 독일 베를린 샤리테 의과대학 연구진은 새로운 연구에서 질병에도 불구하고 간이 박테리아 여과 기능을 어떻게 유지하는지 처음으로 관찰했습니다. 이를 통해 이전에 알려지지 않은 간 질환의 회복 메커니즘을 발견했습니다. 간의 특수 면역 세포인 쿠퍼 세포가 조직 흉터로 인해 손상되면 골수에서 나온 면역 세포가 간으로 흘러가서 더 큰 클러스터를 형성한다는 것입니다.
이러한 발견은 간 손상에 대한 새로운 치료법을 개발하는 데 도움이 될 수 있습니다. 관련 연구 결과는 최근 사이언스(Science) 저널에 "Kupffer cell–like syncytia replenish resident macrophage function in the fibrotic liver"라는 제목으로 게재되었습니다.
Science, 2023 , doi:10.1126/science.abq5202
간경변증 환자의 조직 샘플에서 쿠퍼 세포의 기능을 주의 깊게 연구했습니다. 그 과정에서 그들은 쿠퍼 세포 유사 융합체(Kupffer cell-like syncytia)라고 불리는 새로운 세포 유형을 발견했습니다. 이 세포는 골수에서 유래된 더 큰 다핵 면역 세포 덩어리인 거대 세포의 한 종류입니다.
논문의 공동 제1저자이자 베를린 샤리테 의과대학의 Moritz Peiseler 박사는 간 흉터 및 섬유화 중에 일어나는 일을 다음과 같이 설명했습니다. "점점 더 많은 간 세포가 죽습니다. 결합 조직은 전체 간 기관과 작은 혈관 을 둘러싸고 있습니다 . " 혈액은 간 내부와 주변의 새롭고 확장된 혈관으로 방향이 변경됩니다. 이로 인해 쿠퍼 세포가 주변 환경과의 접촉을 잃게 되어 결국 더 이상 간에서처럼 작동하지 않게 됩니다. 혈액에서 박테리아를 더 오래 유지하면 혈액 내 감염이 증가합니다. 골수의 면역 세포(특화된 단핵구)가 간에 침투하는 데 오랜 시간이 걸리지 않습니다. 이전 구조를 우회하는 측면 혈관을 따라 충분히 큰 세포를 형성합니다. 약간 더 큰 혈관에서 박테리아를 걸러냅니다." 이것은 장내 미생물군집에 의해 촉발되는 형태입니다.
새로 형성된 쿠퍼 세포와 유사한 융합체는 실제 쿠퍼 세포의 필터링 기능을 대신합니다. 변화된 혈관 내에 존재해야 하기 때문에 해당 부위로 이동하는 이러한 면역 세포는 적응하여 효과적인 미생물 필터가 되는 메쉬형 구조를 형성합니다. 새로운 연구에서 저자는 이러한 과정과 관련된 분자 메커니즘을 설명합니다.
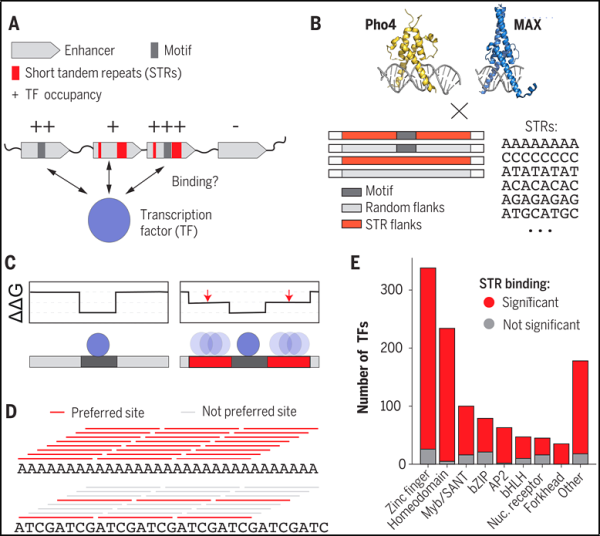
2. Science: 탠덤의 반복으로 인자와 결합 및 유전자 발현을 조정합니다.
연구원들은 "DNA"가 실제로 중요한 역할을 한다는 사실을 수십 년 동안 알고 있었습니다. 게놈의 단백질을 코딩하는 유전자는 단백질을 만드는 기초를 제공하지만, 게놈의 일부 비코딩 부분은 이전에 "정크 DNA"로 간주되었던 게놈 영역을 포함합니다. "는 이러한 유전자의 발현을 증가시키거나 감소시키는 것으로 보입니다. 그러나 특정 비암호화 영역이 유전자 발현 수준에 어떻게 영향을 미치는지는 불분명합니다.
이제 스탠포드 대학 의료 센터의 생명공학 부교수이자 유전학 부교수인 Polly Fordyce 박사와 동료들은 새로운 연구에서 이러한 미스터리 중 일부를 밝혀냈습니다. 그들의 발견은 과학자들이 자폐증, 정신분열증, 암 및 크론병을 포함한 복잡한 유전 질환을 이해하는 데 도움이 될 수 있습니다.
관련 연구 결과가 최근 사이언스(Science) 저널에 "Short tandem repeats bind transcription factors to tune eukaryotic gene expression"라는 제목으로 게재되었습니다.
Science, 2023, doi:10.1126/ science.add1250
Fordyce는 "짧은 탠덤 반복(STR)의 존재 여부가 유전자 발현의 변화와 연관되어 있기 때문에 우리는 정크 DNA가 아니라는 사실을 오랫동안 알고 있었습니다. 그러나 우리는 STR이 어떻게 이러한 영향을 미치는지 몰랐습니다."라고 말했습니다. 새로운 연구에서 저자는 STR 변화가 유전자 발현에 어떻게 영향을 미치는지 이해하기 위한 첫 번째 로드맵을 제공합니다.
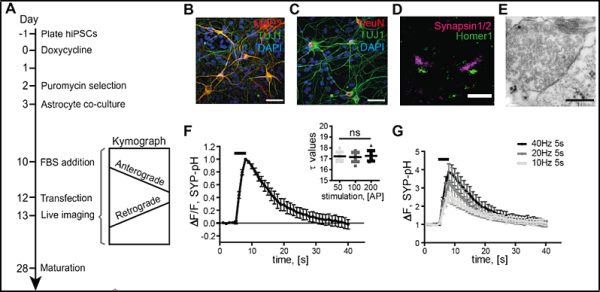
3. Science: 시냅스 형성 메커니즘을 해독하는 새로운 연구
그리고 시냅스후막. 신경 전달 물질은 시냅스 전 막의 시냅스 소포에만 존재하고 시냅스 전 막에서만 방출된 다음 시냅스 후 막에 작용할 수 있으므로 뉴런 간의 흥분 전달은 단방향일 수 있습니다. 이러한 시냅스에서 전기 자극은 인접한 시냅스 후 뉴런이 수신하고 감지할 수 있는 화학적 전달자로 변환됩니다. 정보를 전송하는 것 외에도 시냅스는 정보를 저장할 수도 있습니다. 시냅스의 구조와 기능은 꽤 잘 알려져 있지만, 시냅스가 어떻게 형성되는지에 대해서는 알려진 바가 거의 없습니다.
새로운 연구에서 독일 라이프니츠 분자 약리학 연구소, 베를린 샤리테 의학 연구소, 막스-델브뤼크 분자 의학 센터, 라이프치히 대학교, 미국 시카고 대학교 및 대학의 연구자들은 수수께끼를 풀었습니다.
관련 연구 결과는 사이언스 저널에 2023년 10월 13일자 "Phosphatidylinositol 3,5-bisphosphate facilitates axonal vesicle transport and presynapse assembly"라는 제목으로 게재되었습니다.
Science, 2023, doi:10.1126/ science.adg1075
처음부터 시냅스전 막의 형성을 추적하기 위해 저자는 CRISPR 유전자 가위를 사용하여 형광 단백질을 인간 줄기 세포 에 삽입 하고 조작된 줄기 세포를 사용하여 뉴런을 생성했습니다. 이 형광 라벨을 사용하면 이제 현미경으로 인간 신경 세포 발달 과정에서 초기 시냅스 소포의 발달을 직접 관찰할 수 있습니다.
논문의 교신저자인 폴커 하우케(Volker Haucke) 교수는 “시냅스 소포 단백질과 소위 '활성 영역'에 있는 단백질은 물론 시냅스를 함께 연결하는 접착 단백질도 모두 동일한 버스를 공유한다”고 말했습니다. 그러나 연구 내에서 배양된 인간 뉴런에서 얻은 데이터는 매우 명확해 보였습니다."
그러면 이 단백질들이 시냅스 형성 부위에 정확히 어떻게 도달합니까? 새로운 연구에서 저자들은 모터 단백질 분자 기계가 축삭 수송에 힘을 실어준다는 것을 입증할 수 있었습니다. 그들의 발견에 따르면, 주요 원동력은 KIF1A라는 키네신입니다. 이 운동 단백질은 말초 신경계 와 뇌 의 신경 장애에 관여하는 것으로 가장 잘 알려져 있습니다 .
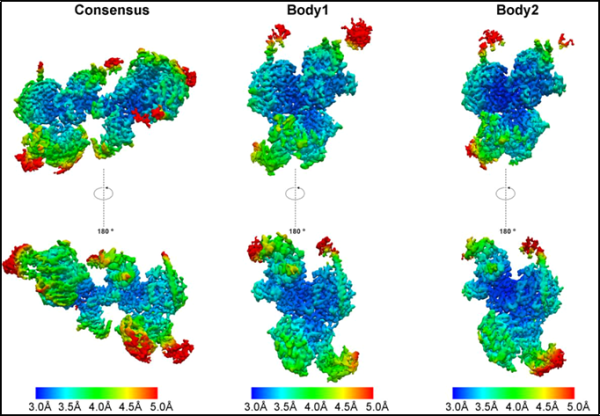
4. Science: PRC2 불활성화를 조절하는 RNA의 메커니즘을 구조적으로 밝힙니다.
모든 인간 세포는 정확히 동일한 유전자 세트를 가지고 있습니다. 우리 세포 깊은 곳에는 PRC2라는 분자 기계가 어떤 세포가 심장 세포가 되고, 어떤 세포가 뇌 세포가 되고, 어떤 세포가 근육 세포나 피부 세포가 되는지를 결정하는 데 중요한 역할을 합니다.
이 분자 기계가 없거나 손상되면 태아가 정상적으로 발달할 수 없습니다. 돌연변이가 발생하면 세포가 통제할 수 없을 정도로 성장하고 암이 발생할 수 있으므로 PRC2는 약물 개발자의 주요 표적이 됩니다.
새로운 연구에서 콜로라도 볼더 대학교와 하버드 의과대학의 연구자들은 PRC2(폴리콤 억제 복합체 2, 폴리콤 억제 복합체 2)가 어떻게 작동하는지, 특히 리보핵산(RNA)이 어떻게 유전자를 활성화하고 또한 비활성화도 제어합니다.
이번 연구 결과는 발달 과정에 대한 새로운 통찰력을 제공하고 혈액암, 췌장암 , 대장암, 백혈병, 소아 종양 등 치료가 어려운 암에 대한 새로운 치료법 개발의 길을 열었습니다 .
관련 연구 결과는 최근 사이언스(Science) 저널에 "Structural basis for inactivation of PRC2 by G-quadruplex RNA"라는 제목으로 게재되었습니다.
Science, 2023, doi:10.1126/science.adh0059
논문의 공동 교신저자이자 콜로라도 볼더 대학교 생화학 조교수인 Vignesh Kasinath는 "우리는 PRC2가 세포 정체성의 발달과 유지에 매우 중요하다는 것을 알고 있으며, RNA가 이를 조절한다는 것도 알고 있습니다.”
이 새로운 연구에서 Kasinath 연구소는 노벨상 수상자 Thomas Cech 및 동료들과 협력하여 최첨단 "저온 전자 현미경" 기술을 사용하여 PRC2의 활동 과정을 촬영했습니다. 이 기술은 샘플을 극저온으로 동결시켜 원래의 구조를 보존한 후, 빛의 속도보다 빠르게 이동하는 전자빔으로 샘플을 조사하여 초고해상도 3차원 이미지를 생성합니다.
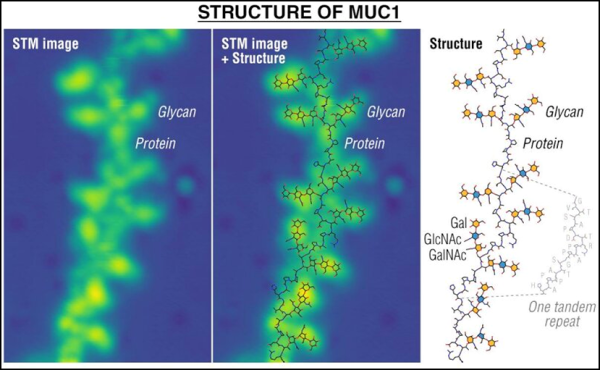
5. Science: 단백질과 지질에 결합된 글리칸의 서열과 위치를 단일 분자 수준에서 직접 관찰합니다.
새로운 연구에서 독일 막스플랑크 고체연구소, 튀빙겐대학교, 덴마크 코펜하겐대학교 연구진은 단일 분자 수준에서 여러 생체분자와 결합된 글리칸(글리칸)의 사진을 찍는 방법을 보고했습니다. -- 다당류라고도 알려져 있음 ---
순서 및 위치 방법 관련 연구 결과는 'Direct observation of glycans bonded to proteins and lipids at the single-molecule level'이라는 제목으로 사이언스지에 2023년 10월 13일 게재됐습니다.
Science, 2023, doi:10.1126/ science.adh3856
글리칸 결합을 이미지화하는 방법을 찾기 위한 광범위한 실험을 수행한 후, 저자는 지질 및 단백질 분자에 결합된 글리칸(글리칸아미노글리칸 및 당접합체라고 함)을 두 금속, 즉 은과 구리의 표면에 결합시키는 전기분무 기술을 발견했습니다. 이를 통해 터널링 현미경을 사용하여 이러한 글리칸 분자를 직접 이미지화할 수 있었습니다. 그들은 글리칸 사슬 내의 특정 단당류를 식별할 수 있었고, 이를 통해 글리칸의 방향과 그것이 단백질 백본에 부착되는 위치를 더 잘 이해할 수 있었습니다.
저자들은 또한 뮤신에 결합된 산소 연결 글리칸의 사진을 획득하여 새로운 이미징 기술을 시연했으며 이러한 사진이 초기 암 바이오마커 검색에 도움이 될 수 있음을 지적했습니다. 이 기술은 다양한 연구 노력에 사용될 수 있으며 알려지지 않은 당지질 및/또는 당단백질의 발견에도 도움이 될 수 있습니다
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.