2023년 Nature Communications:Mitochondrial dysfunction promotes the transition of precursor to terminally exhausted T cells through HIF-1α-mediated glycolytic reprogramming
페이지 정보
작성자 PnH 조회98회 작성일 24-05-31 04:47본문
2023년 Nature Communications:Mitochondrial dysfunction promotes the transition of precursor to terminally exhausted T cells through HIF-1α-mediated glycolytic reprogramming
면역 체계가 암과 감염과 싸울 때 T 세포 고갈이 자주 발생합니다. T 세포가 점차 기능을 잃어 암과 감염에 대한 반응을 방해하는 과정입니다. 이러한 기능 상실을 제어하는 분자 메커니즘은 아직 완전히 이해되지 않았습니다.
면역 체계가 암과 감염과 싸울 때 T 세포 고갈이 자주 발생합니다. T 세포가 점차 기능을 잃어 암과 감염에 대한 반응을 방해하는 과정입니다. 이러한 기능 상실을 제어하는 분자 메커니즘은 아직 완전히 이해되지 않았습니다.
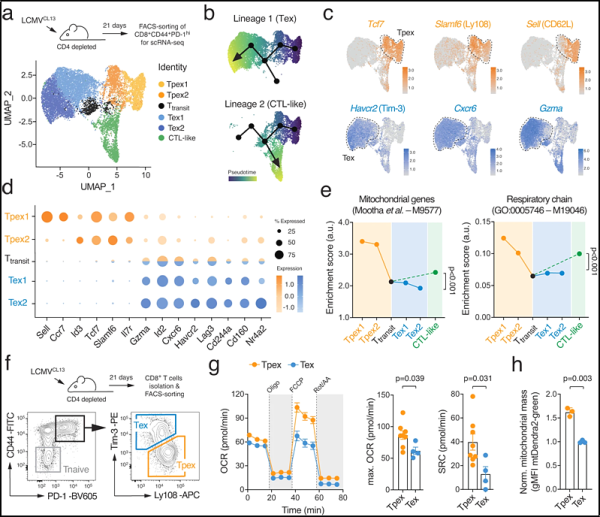
새로운 연구에서 독일 뷔르츠부르크 대학의 면역학자 마틴 바에스(Martin Vaeth)와 그의 연구팀은 이 현상에 대한 가능한 설명을 발견했습니다. 즉, T 세포 고갈 과정은 "세포 에너지 공장" 미토콘드리아의 영향을 크게 받는다는 것입니다. 관련 연구 결과는 2023년 10월 27일 네이처 커뮤니케이션즈(Nature Communications) 저널에 게재되었습니다. 논문 제목은 "미토콘드리아 기능 장애는 HIF-1α 매개 해당과정 재프로그래밍을 통해 전구체가 최종적으로 소진된 T 세포로 전환되는 것을 촉진합니다Mitochondrial dysfunction promotes the transition of precursor to terminally exhausted T cells through HIF-1α-mediated glycolytic reprogramming."
미토콘드리아 기능장애면 일련의 반응이 촉발되어 궁극적으로 T 세포의 유전적 및 대사적 재프로그래밍으로 이어지며, 이는 T 세포 실패를 유발하는 과정입니다. 그러나 T 세포의 이러한 "고갈"은 대응될 수 있습니다. 약물이나 유전학을 통해 세포 대사를 최적화하면 T 세포의 수명을 연장하고 기능을 향상시킬 수 있습니다. 이는 예를 들어 에너지 공급 분자인 아데노신 삼인산(ATP)의 생산을 촉진하는 미토콘드리아 인산염 수송체를 과발현함으로써 달성될 수 있습니다.
예를 들어 CAR-T 세포 치료법은 백혈병 과 림프종 치료에 상당한 효능을 보였습니다 . CAR-T 세포는 혈액암과 싸우기 위해 실험실에서 유전자 변형된 T 세포입니다. 그러나 CAR-T 세포는 고형 종양을 치료할 때 실패하는 경향이 있어 이와 관련하여 성공이 제한됩니다.
Vaeth 박사는 "우리의 실험은 강화된 미토콘드리아 대사가 만성 감염에서 바이러스 특정 T 세포 의 수명과 기능을 향상시킨다는 것을 보여줍니다 . 이 전략은 또한 T 세포 기반 암 면역요법을 강화하는 데 유용한 것으로 보입니다."라고 말했습니다.
Vaeth 박사는 "미토콘드리아(에너지) 대사의 변화가 T 세포 실패의 결과라고 종종 생각됩니다."라고 Vaeth는 말했습니다. Vaeth는 미토콘드리아 기능 장애가 T 세포 실패의 실제 원인임을 확인하기 위해 새로운 유전 모델을 개발했습니다. 이는 인산 수송체 Slc25A3을 차단하여 T 세포의 미토콘드리아를 마비시킵니다.
Nature Communications, 2023, doi:10.1038/s41467-023-42634-3
따라서 이러한 T 세포는 아데노신 삼인산 형태의 생체 에너지 요구를 충족하기 위해 다른 대사 경로, 주로 호기성 해당작용으로 전환해야 합니다. 그러나 이러한 대사적 적응은 T 세포에서 활성 산소종의 생산을 증가시킵니다. 산소 라디칼의 수준이 높아지면 T세포 인자 HIF-1α의 분해가 방지됩니다. HIF-1α 단백질의 축적은 T 세포의 유전적 및 대사적 재프로그래밍을 유도하여 T 세포 고갈을 가속화합니다.
다음으로 Vaeth의 팀은 히스톤의 번역 후 변형, T 세포 대사와 국소 조직 미세 환경의 상호 작용 등을 통해 미토콘드리아 반응이 T 세포의 후생적 프로그래밍에 어떻게 영향을 미치는지 탐구하기를 희망합니다.
Vaeth는 종양 의 영양 공급과 산소 장력이 건강한 조직과 매우 다르기 때문에 이것이 특히 중요하다고 생각하며 T 세포는 이러한 어려운 환경에 적극적으로 대처해야 합니다. 공간 전사체 및 대사체 분석과 같은 신기술의 개발은 조직 미세 환경의 맥락에서 이러한 문제를 체계적으로 고해상도로 연구할 수 있는 흥미롭고 새로운 가능성을 제공합니다.
출처입니다
Hao Wu et al. Mitochondrial dysfunction promotes the transition of precursor to terminally exhausted T cells through HIF-1α-mediated glycolytic reprogramming. Nature Communications, 2023, doi:10.1038/s41467-023-42634-3.
Preventing the Exhaustion of T Cells
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.