2023년 CAR-T 세포치료 12월 발표 요약
페이지 정보
작성자 PnH 조회173회 작성일 24-05-31 05:08본문
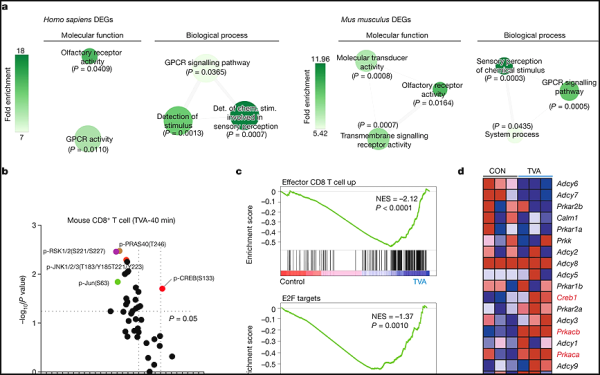
1.Nature: 쇠고기와 유제품에 함유된 트랜스 TVA은 종양에 침투하고 암세포를 죽이는 CD8+ T 세포의 능력을 증가시키는 것으로 밝혀졌습니다.
시카고 대학, 세인트 주드 아동 연구 병원, 에모리 대학 연구진은 새로운 연구에서 소, 양 등 방목 동물의 고기와 유제품에 장쇄 지방산이 함유되어 있다는 사실을 발견했습니다. (TVA) --- 종양에 침투하여 암세포를 죽이는 CD8+ T 세포의 능력을 향상시킬 수 있습니다. 그들은 또한 혈액 내 TVA 순환 수준이 높은 환자가 면역요법에 더 잘 반응한다는 사실을 지적했는데, 이는 TVA가 암의 임상 치료를 돕기 위한 영양 보충제로 사용될 가능성이 있음을 시사합니다. 관련 연구 결과는 2023년 11월 22일 네이처 저널에 온라인 게재됐다. 논문 제목은 '트랜스TVA 재프로그램 CD8+ T 세포 및 항종양 면역'입니다.
Nature, 2023, doi:10.1038/s41586-023-06749-3.
논문의 공동 교신저자이자 시카고 대학교 의학 교수인 Jing Chen 박사는 "식이 요법과 인간 건강 사이의 연관성을 해독하려는 많은 연구가 있지만 사람들이 먹는 음식의 종류가 매우 다양하기 때문입니다. , 근본적인 메커니즘을 이해하는 것은 매우 어렵습니다. 그러나 식품의 영양소와 대사 산물에만 집중하면 생리학 및 병리학에 어떻게 영향을 미치는지 이해할 수 있습니다. T 세포 반응을 활성화하는 영양소에 초점을 맞춤으로써 우리는 다음과 같은 사실을 발견했습니다. 실제로 중요한 면역 경로를 활성화하여 항 종양 면역 반응을 향상시키는 단백질입니다."
Chen 연구실은 혈액 내 순환하는 대사물질, 영양소 및 기타 분자가 암 발병 및 암 치료에 대한 반응에 어떻게 영향을 미치는지 이해하는 데 중점을 두고 있습니다. 새로운 연구에서 두 명의 박사후 연구원인 Hao Fan 박사와 Siyuan Xia 박사는 식품에서 알려진 약 700개의 대사산물 데이터베이스로 시작하여 영양소에서 235개의 대사산물 데이터베이스를 구축했습니다. " 생리활성 분자로 구성된 화합물 라이브러리입니다. 그들은 이 새로운 라이브러리의 화합물을 검사하여 암세포나 바이러스에 감염된 세포를 죽이는 데 중요한 세포 유형인 CD8+ T 세포를 활성화하여 항종양 면역 반응에 영향을 미칠 수 있는지 여부를 결정했습니다.
그들은 인간과 쥐 세포에서 상위 6개 후보 화합물을 평가한 결과 TVA가 가장 잘 수행된다는 사실을 발견했습니다. TVA는 모유에 가장 풍부한 트랜스 지방산이지만 신체가 스스로 생산할 수는 없습니다. TVA의 약 20%만이 다른 부산물로 분해되어 80%가 혈액에 순환됩니다. Chen은 "이것은 그것이 다른 효과를 가져야 한다는 것을 의미하므로 우리는 더 많은 연구를 시작했습니다"라고 말했습니다.
TVA가 풍부한 식이를 먹인 쥐는 대조군 식이를 먹인 쥐에 비해 흑색종 과 결장암 세포의 종양 성장 잠재력을 크게 감소시켰습니다. TVA가 풍부한 식단은 또한 CD8+ T 세포가 종양에 침투하는 능력을 향상시킵니다.
Chen 연구실과 He 연구실에서 실시한 이러한 추가 분석에서는 TVA가 일반적으로 장내 미생물군에 의해 생성되는 단기 단백질에 의해 사용되는 GPR43이라는 세포 표면의 수용체를 비활성화시키는 것으로 나타났습니다. TVA는 이러한 단쇄 지방산을 억제하고 세포 성장, 생존 및 분화와 같은 여러 기능에 관여하는 CREB 경로라는 세포 신호 전달 과정을 활성화합니다. 또한 CD8+ T세포의 GPR43 수용체가 완전히 제거된 모델에서도 항종양 능력이 향상되지 않는 것으로 확인됐습니다.
마지막으로 그들은 시카고 대학의 의학 교수인 저스틴 클라인(Justin Kline) 박사와 협력하여 CAR-T 세포 면역요법으로 치료받은 림프종 환자의 혈액 샘플을 분석했습니다. 그들은 TVA 수준이 높은 환자가 TVA 수준이 낮은 환자보다 치료에 더 잘 반응하는 경향이 있음을 관찰했습니다. 그들은 또한 의학 교수인 Wendy Stock 박사와 협력하여 백혈병 세포주를 테스트한 결과 TVA가 백혈병 세포를 죽이는 면역요법 약물의 능력을 강화한다는 사실을 발견했습니다.
2. Nature: 단일 T세포의 항암반응 맵 확인 면역항암치료법 개발이 기대됩니다.
T 세포는 암을 죽이는 데 관여하는 면역 체계의 핵심 구성 요소입니다. 종양에 의해 생성된 신호는 부분적으로 T 세포가 피로라고 알려진 덜 기능적인 상태로 점진적으로 분화(성숙)하도록 강제함으로써 이러한 T 세포를 차단합니다.
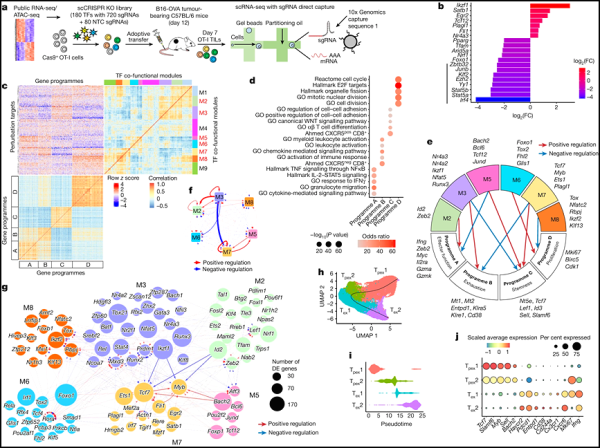
새로운 연구에서 미국 세인트 주드 아동 연구병원(St. Jude Children's Research Hospital) 연구진은 암에서 T세포의 분화 상태에 관여하는 전사인자를 종합적으로 연구했다. 그런 다음 그들은 이 정보를 사용하여 T 세포 분화를 촉진하거나 예방함으로써 전임상 모델에서 항암 활동을 강화했습니다. 이러한 발견은 암 면역치료에 중요한 의미를 갖는다. 관련 연구 결과는 2023년 11월 15일 네이처(Nature) 저널에 온라인으로 게재되었습니다.
논문 제목은 "단일 세포 CRISPR 스크린 생체 내 T 세포 반응 지도 (암)"입니다.
Nature, 2023, doi:10.1038/s41586-023-06733-x.
입양 세포 치료(ACT)에 사용되는 T 세포는 암세포를 표적으로 삼아 죽이는 데 사용됩니다. 효능의 이러한 차이는 부분적으로 T 세포 고갈을 촉진하는 종양에 기인하며, 이는 T 세포가 암세포를 적극적으로 죽이는 데 덜 효율적이게 만듭니다. 저자들은 T 세포 분화 과정을 정확하게 방해하여 항종양 효능을 향상시킬 수 있음을 발견했습니다.
"T 세포는 종양 면역요법의 초석이며, 우리는 T 세포를 더 효과적으로 만들기 위해 재프로그래밍하는 새로운 방법을 찾았습니다. 우리는 T 세포를 특수한 상태로 밀어넣어 더 강력한 종양 살해 세포로 만들 수 있습니다."
3. Nat Commun: 강력한 γδ T 세포 개발, 보편적인 암 면역치료 유망
동종 세포 치료법이라고도 불리는 "기성품" 세포 치료법은 환자가 아닌 건강한 기증자의 면역 세포를 사용합니다. 이 접근 방식을 통해 키메라 항원 수용체(CAR) T세포 치료와 같은 세포 치료를 더 많은 환자가 보다 시기적절하게 이용할 수 있게 될 수 있으며, 이는 환자에게 생명을 구하는 치료법을 제공하는 데 있어 주요 장벽 중 하나입니다.
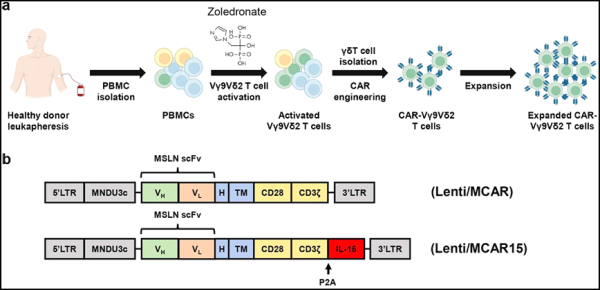
새로운 연구에서 UCLA의 연구자들은 까다로운 질병인 성암을 치료하기 위한 "기성품" 세포 치료법에 잠재적으로 사용될 수 있는 보다 강력한 면역 세포를 조작하는 새로운 방법을 개발했습니다. 이 새로운 접근법은 비용이 저렴하고 대기 시간이 짧으며 대규모로 생산되어 전 세계 병원으로 배송될 수 있는 보다 효과적인 세포 치료법을 개발하기 위한 핵심 단계입니다. 환자의 범위. 관련 연구 결과는 2023년 11월 8일 Nature Communications 저널에 게재되었습니다. 논문 제목은 "CD16 바이오마커 선택 및 CAR/IL-15 엔지니어링을 통해 난소암 치료를 위한 동종 Vδ2 T 세포의 잠재력 잠금 해제"입니다.
Nature Communications, 2023, doi:10.1038/s41467-023-42619-2
논문 교신저자이자 UCLA 미생물학, 면역학, 분자유전학 부교수인 릴리 양(Lili Yang)은 "진행성 암 환자를 치료할 때 시간이 가장 중요한 경우가 많다"며 "현재 이러한 유형의 치료법은 규정에 따라 투약해야 한다"고 말했습니다. 환자의 특정 상태에 따라 맞춤화됩니다. 환자에게서 T 세포라고 불리는 면역 세포를 추출하고, 이 세포를 유전적으로 변형한 다음 다시 환자에게 주입해야 합니다. 이 과정은 각 환자를 치료하는 데 몇 주에서 몇 달이 걸릴 수 있습니다. 비용이 많이 들 수 있습니다. 환자는 수십만 달러를 지불해야 합니다."
새로운 연구에서 Yang과 그녀의 팀은 고형 종양을 포함하여 다양한 암을 표적으로 삼을 수 있지만 이식을 유발하지 않는 것으로 알려진 면역 세포의 일종인 감마 델타 T 세포에 중점을 두었습니다.
감마 델타 T 세포 기반 치료법이 이전에 연구되었지만 기증자 다양성, 일시적인 지속성 및 암세포가 신체의 면역 반응을 회피하거나 회피하는 능력으로 인해 임상적 성공이 제한적이었습니다.
그러나 Yang과 그녀의 팀은 CD16 표면 마커를 높게 발현하는 기증자 γδ T 세포가 암세포를 더 잘 죽일 수 있다는 것을 발견했습니다. 양 교수는 "이러한 CD16 고발현 γδ T 세포는 종양 인식 능력을 향상시키는 독특한 특성을 보인다. 이들은 더 높은 수준의 이펙터 분자를 나타내며 암세포에 대해 항체 의존성 세포독성을 생성하는 능력을 보유하고 있다"고 말했다. CD16을 기증자 선택을 위한 바이오마커로 사용하면 암 특성이 향상될 수 있습니다."
4. Cell: CAAR-T 세포 치료가 자가면역 뇌염 치료에 유망하다는 새로운 연구 결과가 나왔습니다.
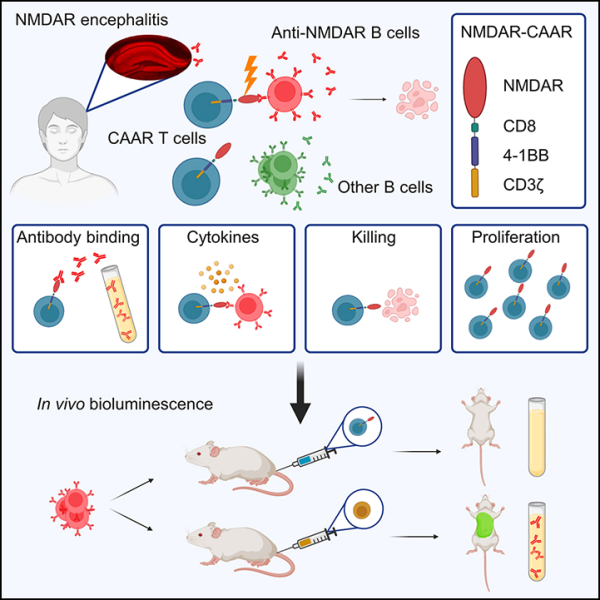
독일 신경퇴행성 질환 센터와 Charité Berlin의 연구자들은 새로운 연구에서 NMDA 수용체 뇌염이라고 불리는 가장 흔한 자가면역 뇌 질환에 대한 치료법을 개척했습니다. 질병을 일으키는 세포를 표적으로 삼아 제거하기 위해 T 세포라고 불리는 백혈구를 재프로그래밍함으로써 이 접근 방식은 새로운 수준의 정확성과 효율성에 도달합니다. 실험실 연구에서는 성공적이었으며 현재 인간을 대상으로 한 임상 시험이 계획되어 있습니다. 관련 연구 결과는 '키메라 자가항체 수용체 T 세포가 NMDA 수용체 특이적 B 세포를 고갈시킨다'라는 제목으로 저널 셀(Cell)에 2023년 11월 1일 온라인 게재됐다.
Cell, 2023, doi:10.1016/j.cell.2023.10.001
NMDA 수용체 뇌염은 항체 유발 뇌질환 중 가장 흔한 질환이다. 이 질환은 항NMDA 수용체 항체가 갑자기 뇌를 공격하고, 뇌는 다시 환자 자신의 신체를 공격합니다. 논문 공동 교신저자인 하랄드 프뤼스(Harald Prüss) 교수는 “전임상 실험에서 이러한 잘못된 표적 항체(항NMDA 수용체 항체)를 형성하는 B세포를 선택적으로 차단하는 데 성공했다”고 말했습니다.
저자들은 환자에게 주입하기 위해 특수 키메라 자가항체 수용체(CAAR) T 세포(CAAR-T)를 설계했습니다. 이렇게 프로그래밍된 CAAR-T 세포는 항NMDA 수용체 항체를 생성하는 B 세포를 높은 정밀도로 인식하고 제거할 수 있습니다. 실험 모델에서 이 혁신적인 접근 방식은 정확성을 입증했습니다.
CAAR-T 세포가 신체에 다시 들어가면 항NMDA 수용체 항체를 생성하는 B 세포를 특이적으로 공격합니다. 이러한 B 세포의 표면 모양으로 인해 CAAR-T 세포는 B 세포와 정확하게 결합하여 죽일 수 있습니다. 중요한 것은 다른 항체를 생성하여 표면 모양이 다른 B 세포는 영향을 받지 않는다는 것입니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.