2023년 간암 치료에 대한 면역치료 연구 논문
페이지 정보
작성자 PnH 조회132회 작성일 24-05-31 05:44본문
최근 몇 년 동안의 연구에 인간 간암 연구 분야에서 많은 성과를 거두었습니다 .
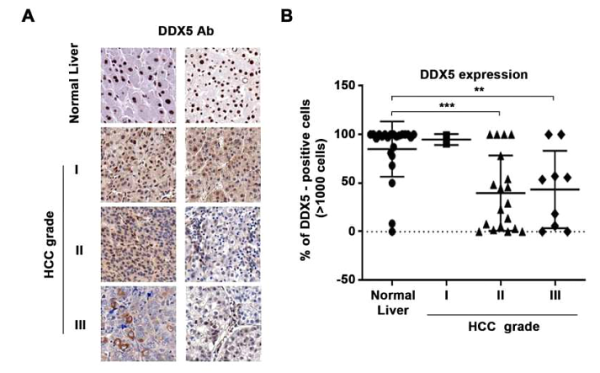
Cell Death & Disease:RNA helicase DDX5 modulates sorafenib sensitivity in hepatocellular carcinoma via the Wnt/β-catenin–ferroptosis axis
최근 간암치료제인 소라페닙과 자연 발생 효소의 관계를 밝혀내는 데 획기적인 진전을 이루었고, 이를 통해 현재 간암만을 치료하고 있는 약의 효과를 높일 수 있게 되었으며, 환자의 기대 수명이 2~3개월 연장되었습니다. , "RNA 헬리카제 DDX5는 Wnt/β-catenin-ferroptosis 축을 통해 간세포 암종에서 소라페닙 민감도를 조절한다"라는 제목의 연구 보고서가 국제 저널 인 Cell Death & Disease에 게재되었습니다. 퍼듀 대학 및 기타 기관의 과학자들은 이들 사이의 연관성을 밝혔습니다. DDX5 효소와 간암치료제 소라페닙에 대한 연구를 통해 기존 항암제 와 DDX5 생성을 촉진하는 치료법을 결합해 간암에 효과적인 치료제로 활용될 수 있을 것으로 기대됩니다.
(2023) DOI:10.1038/s41419-023-06302-0
우라니아 안드리사니(Ourania Andrisani) 연구원 은 “치료 중 간에서 DDX5를 계속 발현할 수 있는 방법을 찾을 수 있다면 소라페닙과 기타 폴리티로신 키나제 억제제가 더 나은 항 종양 효능을 가질 수 있을 것 ”이라고 말했습니다. 간암의 효과적인 치료를 위한 새로운 치료법 개발을 생각해 보세요. 전 세계적으로 매년 75만 명 이상이 간암으로 사망하고 있으며, 부유한 국가에서도 간암 환자의 생존율은 여러 유럽 국가의 10% 미만, 일본의 30%에 이르기까지 낮습니다. 전 세계 간암 사례의 절반 이상이 B형 간염 바이러스의 만성 감염으로 인해 발생합니다. 이제 연구자들은 바이러스 생합성에서 RNA 파괴 단백질의 일종인 DDX5가 수행하는 핵심 역할을 밝히고 있습니다. 자이라제는 변형이 가능한 특수 단백질 입니다. RNA의 구조는 RNA 생물학의 모든 측면에 관여합니다.
이번 최신 연구에서 연구진은 소라페닙으로 치료받은 환자의 간암 . 연구진은 DDX5 수치가 높은 환자가 낮은 환자보다 더 오래 사는 경향이 있다는 사실을 발견했으며, 소라페닙 자체가 간암 세포와 간암 동물 모델에서 의식적으로 DDX5를 감소시킬 수 있다는 사실을 발견했습니다. 동일한 수준에서 RNA 염기서열분석 결과에 따르면 이 약물은 활성화될 수 있습니다 간 배아 발달에서 일반적으로 활성화되는 일련의 분자 단계인 Wnt/β-카테닌 경로의 필수 유전자입니다. 부적절한 활성화가 발생하면 종종 간암과 직접적으로 관련됩니다.
Cell:Arginine reprograms metabolism in liver cancer via RBM39
암세포는 대사 상태를 완전히 바꾸고 계속해서 성장하는 카멜레온인데, 최근 스위스 바젤대학교 등 연구진이 국제잡지 Cell 에 게재한 'Arginine reprograms Metabolin in Liver Cancer via RBM39'라는 제목의 연구 보고서를 발표했습니다. 과학자들은 높은 수준의 아미노산 아르기닌이 대사 재프로그래밍을 촉진하고 종양 성장을 촉진할 수 있다는 사실을 연구를 통해 발견했으며, 관련 연구 결과는 인간 간암 치료를 개선하기 위한 새로운 치료법 개발에 도움이 될 것으로 기대됩니다. 간은 인체 내에서 많은 중요한 기능을 수행하는 핵심 기관으로, 영양분의 대사, 에너지 저장, 혈당 조절 등의 기능을 하며 해독, 유해 성분 및 약물 제거에 중요한 역할을 합니다. 간암은 가장 흔한 종류의 암 중 하나이며, 간암을 유발하는 요인으로는 비만, 과도한 음주, C형 간염 감염 등이 있으며, 간암 환자의 치료를 향상시키기 위해서는 조기 진단 과 적절한 치료 전략이 매우 중요합니다.
지난 10년 동안 과학자들은 암의 다각적인 특성을 이해하는 데 상당한 진전을 이루었습니다. 오랫동안 세포 증식 장애로 여겨졌던 암이 실제로 세포 증식 장애라는 증거가 늘어나고 있습니다. 즉, 암은 세포가 대사를 재배치하고 통제되지 않은 세포 증식을 허용할 때 발생하는데, 세포는 어떻게 대사를 변화시키고 이러한 변화가 어떻게 종양으로 이어지는 걸까요? 본 연구에서 연구자들은 간암 세포의 대사 재배열을 촉진하는 핵심 동인을 발견했습니다.
건강한 간세포는 암세포로 변하면서 점차 행동을 변화시켜 신진대사를 재프로그램하여 가능한 한 빨리 성장하도록 하고, 정상 세포가 필요로 하는 것보다 더 많은 포도당을 섭취하고 영양분 흡수를 강화합니다. 연구원인 Dirk Mossmann 박사는 "우리는 생쥐와 환자의 간 종양 샘플을 조사하고 분석한 결과, 암세포가 아르기닌을 거의 또는 전혀 생산하지 않음에도 불구하고 종양 샘플에서 아르기닌 수치가 상승했다는 사실을 발견했습니다."라고 연구원인 Dirk Mossmann 박사는 말했습니다 .
Cellular and Molecular Gastroenterology and Hepatology:he origin and fate of liver myofibroblasts
간 섬유증은 반흔 조직이 간의 손상된 세포를 대체할 때 발생합니다. 시간이 지남에 따라 축적된 반흔 조직이 간을 뒤틀어 혈액 공급을 방해하고 점차적으로 간경화 에서 간부전 및 그 이상으로 진행될 수 있습니다. 경우에 따라 간암이 악화될 수 있습니다. 진행성 간질환 환자의 유일한 치료법은 장기이식뿐입니다.
최근 국제학술지 Cellular and Molecular Gastroenterology and Hepatology 에 '간 근섬유아세포의 기원과 운명'이라는 제목의 연구보고서가 게재됐으며, 캘리포니아대학교 샌디에이고 의과대학 등 여러 기관의 과학자들이 연구를 통해 간 근섬유아세포에 대해 기술했다. 간의 흉터 조직을 형성하는 특수 세포인 간 근섬유아세포의 기원과 운명, 그리고 최근 증거에 따르면 가능한 원인 요인을 제거하면 간 섬유증이 역전될 수 있음이 시사됩니다.
"간 섬유증은 바이러스성 간염부터 과도한 알코올 섭취에 이르기까지 건강한 회복보다는 간의 기능을 손상시키고 간의 상처를 초래하는 다양한 요인에 의해 부분적으로 발생할 수 있기 때문에 매우 흔합니다."라고 연구원인 Brenner 박사는 말했습니다. , 비알코올성 지방간 질환(NAFLD)은 미국 인구에게 매우 흔합니다. 실제로 NAFLD는 전 세계 인구의 약 4분의 1에 해당하는 약 10억 명의 건강에 영향을 미치는 것으로 추정되며, NAFLD 환자의 약 20%는 더욱 심각한 형태의 비알코올성 지방간염(NASH)으로 진행됩니다. , 그 주요 특징은 간 염증, 섬유증 및 간경변입니다.
이번 연구에서 연구진은 근섬유아세포가 정상적이고 건강한 간에는 발견되지 않지만, 만성 간 손상(과도한 음주 등)에 반응하여 활성화되어 염증 반응을 유도하는 간성상세포(aHSC)의 활성화를 설명합니다. 상대적으로 희박하고 정지된 비타민 A 저장 세포에서 흉터 형성 단백질을 분비하는 증식성 근섬유아세포로 전환됩니다. 이러한 근섬유아세포는 비기능성 흉터 조직의 철망 구조를 형성하는 것으로 시작됩니다. 이 조직은 시간이 지남에 따라 두꺼워지고 합쳐져 간을 막히게 하고 다른 생명을 위협하는 상태를 유발할 수 있습니다.
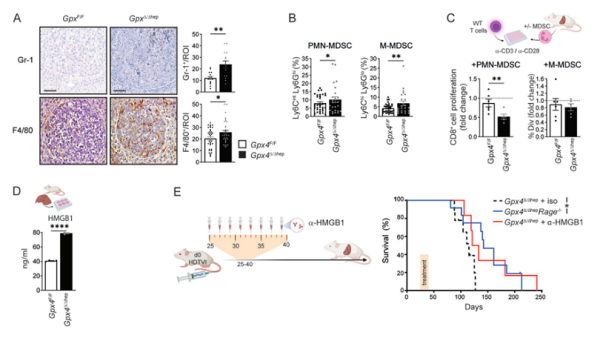
Gut:Combining ferroptosis induction with MDSC blockade renders primary tumours and metastases in liver sensitive to immune checkpoint blockade
10년 전, 철 의존성 세포 사멸, 즉 페롭토시스(ferroptosis)라는 새로운 유형의 프로그램된 세포 사멸이 발견되었습니다. 오랫동안 알려진 프로그램화된 세포 사멸 유형인 세포사멸(apoptosis)과 달리, 페롭토시스(ferroptosis) 세포는 다량의 철분을 섭취합니다. 이 철분은 세포 내에서 대사되어 궁극적으로 세포막을 파괴하게 됩니다. 이러한 유형의 세포 사멸은 발달 과정 및 결함이 있거나 퇴화된 세포의 제거와 같은 신체의 중요한 제어 메커니즘 중 하나입니다. 수년에 걸쳐 면역요법은 암과의 싸움에서 치료 옵션으로 등장했습니다. 면역요법에서는 신체의 자체 방어 시스템이 암세포와 싸우도록 자극됩니다. 이러한 면역요법 중 일부는 시스템을 억제하는 면역 시스템의 면역 체크포인트를 성공적으로 표적으로 삼습니다.
면역관문은 T세포(항암 면역세포) 표면에 있는 일종의 '오프 스위치'로, 이를 통해 T세포의 활동이 하향 조절됩니다. 이 "끄기 스위치"는 특정 "핵심" 단백질에 의해 작동됩니다. 많은 종양은 T 세포의 공격으로부터 자신을 보호하기 위해 이러한 "핵심" 단백질을 형성합니다. 이것이 바로 이 "오프 스위치"를 차단하여 작동하는 면역 체크포인트 억제제라는 약물이 이제 일부 유형의 암에 대한 표준 치료법의 일부가 된 이유입니다. 불행하게도 간암과 같은 다른 유형의 암에서는 면역관문 차단에 대한 반응이 낮습니다.
최근 국제학술지인 Gut 에 게재된 "Combining ferroptosis induction with MDSC blockade renders 원발성 종양과 전이성 간의 간 전이가 면역관문 차단에 민감해진다"라는 제목의 연구 보고서에서 프랑크푸르트 대학병원을 비롯한 여러 기관의 연구자들은 결핵 환자들이 관찰되는 것을 보고했습니다. 직장암 에 걸린 생쥐에서 페 롭토시스(ferroptosis)를 유발하는 물질이 특정 면역 세포(T 세포)를 활성화시키는 것으로 나타났습니다. 이렇게 활성화된 T 세포는 체계적으로 암세포를 죽일 수 있습니다.
Gut , 2023, doi:10.1136/gutjnl-2022-327909
문제는 두 가지 독립적인 메커니즘이 T 세포의 활동을 즉시 다시 차단한다는 것입니다: 첫째, 암세포는 T 세포의 "오프 스위치"(면역 체크포인트 수용체 PD-L1)를 작동하는 "핵심" 단백질을 형성하고, 둘째, 다른 세포 면역체계의 일부인 골수억제세포(MDSC)가 등장하는데, 이 세포의 임무는 신체의 면역 반응을 억제하는 것이기도 합니다. 그러나 저자들이 페로프토시스 활성화제, 면역 관문 억제제, 골수억제 세포 동원을 차단하는 물질의 삼중 조합을 질병에 걸린 쥐에게 주사했을 때 간 종양 성장이 크게 감소했습니다. 쥐를 대상으로 한 추가 테스트에서 저자들은 삼중 병용 요법이 전이성 대장 종양에서 발생하는 간 전이의 수를 줄일 수도 있다는 것을 확인했습니다. 그러나 대장암 자체는 이 삼중 병용요법에 반응하지 않았습니다.
Molecular Cancer:Lysyl hydroxylase LH1 promotes confined migration and metastasis of cancer cells by stabilizing Septin2 to enhance actin network
암 전이는 암 관련 사망의 주요 원인입니다. 최근 국제학술지 Molecular Cancer 에 게재된 "Lysyl hydroxylase LH1은 Septin2를 안정화시켜 암세포의 제한된 이동과 전이를 촉진한다"는 제목의 연구 보고서에서 중국 홍콩 시립대 등 여러 기관의 과학자들이 연구를 진행한 바 있습니다. 간암과 췌장암 세포의 이동과 전이를 유발하고 환자의 생존 기간을 단축시키는 단백질이 발견됐습니다. 이러한 발견은 시험관 내 및 생체 내 모델에서 검증되었으며 임상 데이터에 의해 뒷받침되었으며 암 치료를 위한 새로운 잠재적 표적을 제공할 것으로 예상됩니다.
연구자들은 암 전이가 복잡한 과정이라고 말했습니다. 종양 및 주변 조직의 경화증 정도는 종양 성장에 따라 증가하며, 이는 다양한 암 유형에서 종양 세포 이동 및 전이를 위해 제한된 공간, 즉 채널형 기공 경로를 생성하는 것으로 알려져 있습니다. 그러나 제한된 공간에서의 이러한 이동(이하 제한된 이동이라고 함)의 메커니즘은 아직 명확하지 않습니다. 우리의 목표는 암 전이 메커니즘을 더 깊이 파고들어 이와 관련된 새로운 유전자와 단백질을 식별하는 것입니다.
간암의 가장 흔한 유형인 간세포암종 (HCC)은 세계에서 암 사망의 두 번째 주요 원인입니다. 췌관 선암종(PDAC)은 5년 생존율이 10% 미만인 또 다른 매우 공격적인 암입니다. 두 암 모두 고형 종양의 전형적인 특징, 즉 암세포가 이동하도록 허용하는 제한된 기공 또는 채널과 같은 트랙을 포함하는 세포외 기질(ECM)의 과도한 침착을 공유합니다. 따라서 이 저자들은 연구 대상으로 이 두 가지 다른 암 유형을 선택했습니다.
저자는 먼저 분석을 위해 각각 153명과 63명의 환자로부터 HCC 및 PDAC 샘플을 수집했습니다. 이 저자들은 수술 전에 화학요법이나 방사선요법을 받지 않았습니다. 그들은 또한 국립보건원(National Institutes of Health)으로부터 인간의 간암과 췌장암 세포주를 입수했습니다. 양 교수는 “복잡한 암 미세환경을 시뮬레이션하는 것이 가장 큰 과제”라며 “그러나 현재 제한된 환경에서의 세포 이동에 대한 연구 모델이 부족하다”고 설명했다. 세포 이동 과정을 종합적으로 연구하기 위한 3차원 체외 및 생체 내 모델입니다."
Nature Cancer:SULT1A1-dependent sulfonation of alkylators is a lineage-dependent vulnerability of liver cancers
간내 담관암종 및 간세포암종을 포함한 성인의 간 악성종양은 전 세계적으로 암 관련 사망의 두 번째 주요 원인이며, 대부분의 환자는 화학요법이나 면역요법, 또는 이 둘의 조합을 받고 있으며 특정 바이오마커를 선택할 수 없습니다. 최근 국제잡지 네이처 암(Nature Cancer) 에 게재된 "SULT1A1 의존성 알킬화기의 술폰화는 계통 의존성 간암의 취약성이다"라는 제목의 연구 보고서에서 국립보건원(National Institutes of Health) 및 기타 기관의 과학자들은 연구를 통해 문제를 해결했습니다. 인간의 간암과 싸우는 새로운 전략이 발견되어 연구자들이 새로운 항암제를 개발하는 데 도움이 될 수 있습니다. 세포와 쥐를 대상으로 한 일련의 실험을 통해 연구자들은 간암 세포에서 생산되는 특수 효소가 간암의 한 종류를 전환시킬 수 있음을 발견했습니다. 화합물은 항암제로 바뀌며 동물 신체의 암세포를 죽이고 질병의 심각성을 줄일 수 있습니다.
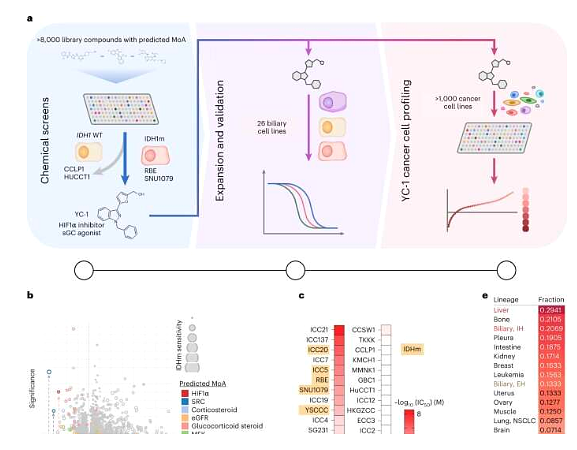
Nature Cancer (2023) DOI:10.1038/s43018-023-00523-0
연구자들은 이 효소가 간암이나 다른 유형의 암에 대한 신약 개발을 돕는 잠재적인 표적이 될 수 있다고 제안합니다. 매튜 홀 박사는 "우리는 특별한 방법으로 희귀한 간암 세포를 죽일 수 있는 특수 분자를 발견했다"며 "이 분자는 인간 간암 세포를 선택적으로 죽일 수 있는 화합물을 스크리닝하는 과정에서 선택됐다"고 말했습니다. 이를 발견하기 위해 많은 노력이 필요하며 간암 세포의 효소에 의해 전환되어 독성 항암제를 생산할 수 있습니다.
바르디시 연구원은 당초 인체의 담관에 영향을 미치는 간암의 일종인 인간 담관암 종을 연구했는데, 주요 특징은 IDH1 효소의 돌연변이이기 때문에 연구진은 연구를 통해 IDH1 돌연변이에 효과적으로 저항할 수 있는 특수 화합물과 약물을 찾고자 했습니다. 수많은 공동 연구를 통해 연구자들은 IDH1을 표적으로 삼아 담관암종 세포를 죽이는 데 있어 승인된 수천 가지 약물과 실험적 항암제의 효과를 신속하게 테스트할 수 있습니다. 그래서 연구자들은 YC-1을 포함한 다양한 분자가 암세포를 죽일 수 있다는 사실을 발견했지만, YC-1이 어떻게 작동하는지 알고자 했을 때 그 화합물이 IDH1 돌연변이에 영향을 미치지 않을 수도 있다는 사실을 발견했습니다.
Journal of Hepatology:ATF4 suppresses hepatocarcinogenesis by inducing SLC7A11 (xCT) to block stress-related ferroptosis
간암은 인간의 암 사망 원인 중 세 번째이자 전 세계적으로 여섯 번째로 흔한 암 유형입니다. 주요 위험 요인으로는 비만, 바이러스성 간염, 지방간염(지방간 및 염증성 간 질환)과 같은 환경 및 대사성 스트레스 요인이 있습니다. 스트레스는 간세포(간의 주요 세포 유형)를 죽임으로써 간을 손상시킵니다. 그에 따른 세포 사멸은 염증 반응을 유발하고 간에 신호를 보내 새로운 간 세포 배치를 생성하도록 합니다. 그러나 이러한 갑작스러운 압박 세포 증식은 또한 종양의 위험을 증가시킵니다.
최근 국제학술지 Journal of Hepatology 에 게재된 "ATF4는 SLC7A11(xCT)를 유도하여 스트레스 관련 페롭토시스를 차단함으로써 간암 발생을 억제한다"는 제목의 연구 보고서에서 상하이 중의과대학 및 기타 기관 과학자들이 연구를 통해 조사한 핵심적인 역할을 하고 있다. ATF4 활성화 전사 인자 4(ATF4, 활성화 전사 인자 4) 중 ATF4는 간 스트레스 반응의 핵심 중재자입니다. 이전 연구에서는 이것이 진행성 간암의 발병과 관련이 있다는 것이 밝혀졌지만 연구자들은 ATF4가 일반적으로 간 면역을 보호한다는 사실을 발견했습니다. 간세포의 죽음과 그에 따른 종양 형성에서 영감을 얻은 이 예상치 못한 결과는 과학자들이 간 질환과 암의 발병을 예방하기 위한 새로운 임상 전략을 개발하도록 영감을 줄 것으로 예상됩니다.
ATF4 수치는 일반적으로 건강한 세포에서는 낮지만 세포가 스트레스를 받으면 수치가 증가합니다. 간암 진행에서 ATF4의 주요 역할을 연구하기 위해 연구진은 ATF4가 결핍된 간세포 모델을 갖춘 쥐를 개발한 후 쥐를 다음과 같은 환경에 노출시켰습니다. 다양한 스트레스가 간 손상과 종양 형성을 촉진합니다. 연구자들은 ATF4가 결핍된 쥐가 더 많은 간 세포 사멸, 염증, 보상 세포 증식을 보이고 간암 발병을 가속화하는 경향이 있다는 사실을 발견하고 매우 놀랐습니다. 어떤 방식으로든 간암 발생으로부터 신체를 보호할 수 있습니다.
Cell Genomics:Single Nucleus RNA Sequencing of Pre-Malignant Liver Reveals Disease-Associated Hepatocyte State with HCC Prognostic Potential
현재의 만성 간 질환 병기 결정 방법은 신체의 간암 위험 예측에 제한적으로 사용되는 경우가 많으며, 최근 국제 저널인 Cell Genomics 에 "Single Nucleus RNA Sequencing of Pre-Malignant Liver Reveals Disease-Associated Hepatocyte State"라는 제목의 논문이 게재되었습니다. HCC 예후 가능성(HCC Prognostic Potential) 연구 보고서를 통해 커틴 대학(Curtin University) 및 기타 기관의 과학자들은 전암성 악성 간세포의 유전적 특징을 확인했는데, 이는 매년 호주에서 진단되는 치명적인 암 환자 약 3,000명에게 고유한 잠재적으로 중요한 특징입니다.
간 질환 환자의 전암성 세포에 대한 정량 분석은 개인의 향후 간암 위험을 결정하는 데 도움이 될 수 있으며, 만성 간 질환 환자의 암 위험에 따라 단계를 결정하고 모니터링하는 방식을 잠재적으로 바꿀 수 있는 발견이라고 연구자들은 말합니다. . Rodrigo Carlessi 박사는 이번 연구에서 가장 진보된 기술을 사용하여 한 번에 수천 개의 유전자의 분자 지문을 한 번에 하나씩 식별했으며 그 과정에서 유전적 특징과 진단 가치를 발견했으며 이후에도 수백 명의 개별 환자 간 샘플에서 확인되었습니다.
이번 발견은 현재 호주 전체 암 관련 사망의 10%를 차지하는 간암을 진단하기 위한 검사 개발의 길을 닦을 수 있는 퍼즐의 중요한 조각을 연구자들에게 제공한다는 점에서 중요합니다. 간암은 일반적으로 호주 인구에서 진행된 단계에서 발견됩니다. 쉽게 이용할 수 있고 정확한 실험실 검사나 바이오마커가 부족하기 때문에 진행성 간암에 걸린 많은 환자의 생존 기간은 대개 12개월 미만입니다. 간암이 발견된 진행 단계, 이때 환자의 치료 옵션은 매우 제한적인 경우가 많습니다.
Chinese Medical Journal:Oncogenic β-catenin-driven liver cancer is susceptible to methotrexate-mediated disruption of nucleotide synthesis
간암은 세계에서 가장 흔하고 치명적인 암 중 하나입니다. 대부분의 환자는 진행된 단계에서 진단되므로 치료 옵션이 거의 없습니다. 불행하게도 진행성 간세포암종(HCC) 치료를 위한 1차 약물은 그렇지 않을 수도 있습니다. 효과적이지 않으며, 임상치료 이익도 높지 않습니다. 지난 몇 년 동안 과학자들은 특정 유전적 이상과 그것이 질병의 발현 및 진행에 영향을 미치는 방식을 분석하여 간세포암종에 대한 새로운 치료법을 개발하려고 노력해 왔습니다. CTNNB1은 간세포암종에서 가장 흔히 돌연변이가 발생하는 유전자입니다. 베타-카테닌이라고 불리는 단백질; 이 단백질의 돌연변이 버전은 분해에 저항하여 영향을 받은 세포에 축적을 촉진하고 시간이 지남에 따라 과잉 베타를 촉진합니다. -카테닌은 Wnt 신호 전달 경로의 조절 장애를 촉진하여 통제할 수 없는 세포 증식을 유발합니다. 현재 β-카테닌 관련 경로를 표적으로 하는 승인된 치료법은 없습니다.
이러한 배경에서 최근 국제잡지 인 Chinese Medical Journal 에 게재된 "발암성 β-카테닌 유발 간암은 메토트렉세이트 매개 뉴클레오타이드 합성 중단에 취약하다"라는 제목의 연구 보고서에서 중국과학원 및 기타 기관의 연구진은 과학자들은 다른 접근법을 취하여 현재의 화학요법 약물이 베타-카테닌 활성화 간암 치료에 효과적일 수 있는지 여부를 결정하기 시작했습니다. 오래된 약물을 재활용하는 것은 약물 개발의 전체 비용을 줄이고 개발 시간을 단축시키기 때문에 매력적인 전략입니다.
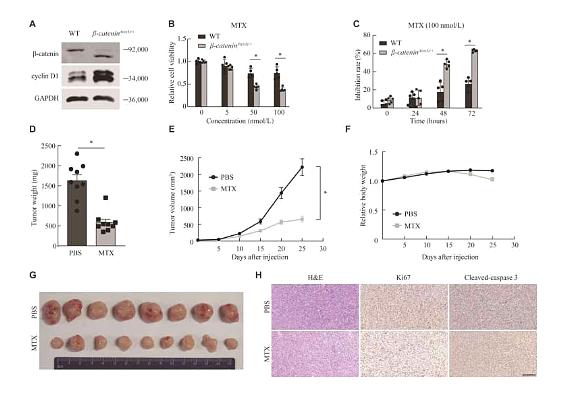
(2023) DOI:10.1097/CM9.0000000000002816
이 목표를 달성하기 위해 연구진은 먼저 돌연변이 CTNNB1 유전자를 발현하는 피하 종양을 접종한 쥐와 배양 중인 유전자 변형 세포를 사용하여 널리 사용되는 12가지 화학요법 약물을 사용하여 스크리닝 테스트를 실시했으며, 널리 사용되는 약물인 메토트렉세이트(MTX)가 널리 사용되는 약물임을 발견했습니다. 건선 , 류마티스 관절염 및 특정 유형의 암과 같은 상태를 치료하는 데 사용되는 약물 은 베타카테닌 활성화 세포에 효과적일 수 있습니다.
Advanced Science:Small Extracellular Vesicle‐Derived vWF Induces a Positive Feedback Loop between Tumor and Endothelial Cells to Promote Angiogenesis and Metastasis in Hepatocellular Carcinoma
간세포 암종은 주로 종양 유래 소형 세포외 소포(sEV)의 조절에 의해 성장과 전파가 주도되는 고도의 혈관성 악성종양입니다. 최근 중국 홍콩대학교의 국제잡지 인 Advanced Science 에 "Small Extracelluo Vesicle-Derived vWF Induces a Positive Feedback Loop between Tumor and Endothelial Cells to Promote Angiogenic and Metasis in Hepatoocyte Carcinoma"라는 연구 보고서가 국제학술지 Advanced Science에 게재되었습니다. 과학자들은 연구를 통해 간암 환자에서 유래한 순환하는 작은 세포밖 소포체에 의해 매개되어 간암 전이를 촉진하는 알려지지 않은 특수 신호 전달 경로를 밝혀냈으며, 이 연구 발견은 과학자들이 인간 간암 치료법 개발에 도움을 줄 수 있을 것으로 기대됩니다.
홍콩에서 간암은 인구 중 5번째로 흔한 암 유형이자 암 관련 사망의 3번째 주요 원인이며 고도의 혈관성 종양으로서 종양 미세환경의 작은 세포외 소포에 의해 종종 발생하는 경우가 많습니다.조절인자에 의해 발생합니다. 강화된 혈관화는 종양 세포가 혈액으로 들어가는 것을 촉진하고 암 전이를 달성하기 위해 인근 부위로의 전파를 촉진합니다. 요즘 점점 더 많은 연구 증거에 따르면 종양 유래 작은 세포외 소포가 혈관 신생 신호 전달 과정에서 중요한 역할을 한다는 것이 밝혀졌습니다. 간암에서 작은 세포외 소포에 의한 혈관신생 조절 뒤에 있는 분자 메커니즘을 이해하는 것은 과학자들이 새로운 치료 전략을 개발하는 데 도움이 될 수 있습니다.
논문에서 연구진은 간세포암종 대상자와 환자를 대상으로 순환하는 작은 세포밖 소포체에 대한 단백질체학 분석을 실시한 결과, von Willibrand 인자(vWF)가 간암 발병 단계에서 점진적으로 상향 조절될 수 있음을 발견했으며, 간암의 급격한 증가를 발견했습니다. 진행성 간암 환자에서 작은 세포외 소포체-vWF의 수준은 간암의 비침습적 진단 마커로 사용될 수 있음을 나타낼 수 있습니다. 간암 간암의 발생 및 전이에서 세포밖 소포체의 유도 능력은 간암에서 작은 세포밖 소포체-vWF의 핵심 역??