2024년 30억 달러 규모 협력 종료, Genentech, TCR-T 세포 치료제 개발 포기
페이지 정보
작성자 PnH 조회119회 작성일 24-05-31 07:34본문
2024년 30억 달러 규모 협력 종료, Genentech, TCR-T 세포 치료제 개발 포기
이번 2상 임상시험에는 북미와 유럽의 23개 의료센터에서 활막육종 환자 44명, MRCLS 환자 8명 등 총 52명의 환자가 참여했습니다. 환자의 36%(19/52)가 치료에 반응하여 종양이 줄어들거나 어떤 경우에는 완전히 사라졌습니다.
최근 Roche의 자회사 Genentech는 Adaptimmune Therapeutics와 30억 달러 규모의 세포 치료 협력 계약을 종료했다고 발표했습니다.
이번 협력은 2021년 Genentech가 Adaptimmune에 1억 5천만 달러의 선불 현금 지불과 3,500만 달러의 마일스톤 지불을 통해 체결되었습니다. 양사는 인간 iPSC를 기반으로 한 동종 T세포 치료제 2종을 개발하기 위해 협력하고 있다. 하나는 최대 5개 표적을 표적으로 하는 기성 치료제이고, 다른 하나는 환자에게서 분리한 αβ T세포 수용체를 활용한 맞춤형 치료제입니다.
이 협력 종료를 발표하기 직전에 Genentech는 직원의 3%를 해고하겠다고 발표했습니다. 올해 초 Genentech의 모회사인 Roche는 Genentech의 제품 개발팀을 축소하겠다고 발표했습니다. Genentech는 일부 협력 프로젝트의 해고 및 종료를 통해 Genentech가 환자에게 가장 큰 영향을 미칠 수 있는 영역으로 자원을 이동할 수 있게 될 것이라고 말했습니다.
Adaptimmune의 경우, GlaxoSmithKline(GSK)은 2023년 3월 두 가지 프로젝트에 대한 협력도 종료했으며, 그 중 하나는 한때 선도적인 세포 치료 프로젝트로 여겨졌던 NY-ESO-1을 표적으로 하는 TCR-T 세포 치료인 lete-cel이 현재 진행 중인 프로젝트입니다. 2상 임상시험 중. 또한 2023년 11월 어댑트뮨은 (gavoo-cel)과 TC-510이라는 두 가지 연구개발 프로젝트도 자체적으로 종료했습니다. 종료 이유는 안전성과 효율성이 부족했기 때문입니다.
Adaptimmune의 CEO인 Adrian Rawcliffe는 회사가 파트너인 Genentech와 매우 귀중한 협력 관계를 유지해 왔으며 회사의 iPSC 기반 동종이계 세포 치료 플랫폼의 장기적인 잠재력에 대해 확신을 갖고 있다고 말했습니다. 지난 12개월 동안 회사는 후기 단계 임상 개발 프로그램인 afami-cel에 집중해 왔습니다.
현재 어댑티뮨은 진행성 윤활막육종 치료를 위한 아파미셀(afami-cel) 치료제에 주력하고 있으며 , 이 TCR-T 치료제는 FDA 로부터 우선 심사를 받았으며 올해 8월 4일 FDA에서 결정이 내려질 것으로 예상됩니다.
2024년 3월 24일, Adaptimmune은 Memorial Sloan Kettering Cancer Center, Washington University School of Medicine, University of Texas MD Anderson Cancer Center 및 기타 기관의 연구원들과 함께 The Lancet 에 진행성 윤활막 육종에 대한 Afamitresgene Autoleucel이라는 제목의 논문을 발표했습니다.
점액성 원형 세포 지방육종(SPEARHEAD-1): 국제 공개 라벨 제2상 시험의 임상 연구 논문을 발표했습니다.
이 국제 공개 라벨 제2상 임상 시험에서 TCR-T 세포치료제 afami-cel은 진행성 윤활막육종 및 점액성 원형 세포 지방육종 (MRCLS) 환자에게 지속적인 반응을 보였습니다 . 이 임상 시험은 TCR-T 세포 치료법이 고형 종양을 효과적으로 표적으로 삼을 수 있음을 입증하고 이 접근법을 다른 고형 악성 종양 으로 확장하는 근거를 제공합니다 .
대부분의 윤활막 육종 및 점액성 원형 세포 지방육종(MRCLS)의 경우 종양 세포는 MAGE-A4라는 단백질을 발현합니다. 이 치료법은 환자로부터 T 세포를 추출하고 렌티바이러스 벡터를 사용하여 유전자 조작을 통해 고친화도 및 특정 T를 발현합니다. - HLA-A*02에 의해 제시된 MAGE-A4 230-239 GVYDGREHTV의 세포 수용체(TCR)는 T 세포가 MAGE-A4 발현 암세포를 표적으로 삼아 이들 암세포를 제거하도록 유도합니다.
이번 2상 임상시험에는 북미와 유럽의 23개 의료센터에서 활막육종 환자 44명, MRCLS 환자 8명 등 총 52명의 환자가 참여했다. 환자의 36%(19/52)가 치료에 반응하여 종양이 줄어들거나 어떤 경우에는 완전히 사라졌습니다. 이 치료법은 MRCLS 환자보다 윤활막육종 환자에서 더 효과적입니다. 평균적으로 반응 기간은 윤활막육종 환자의 경우 11개월이 조금 넘었고 MRCLS 환자의 경우 4개월이 조금 넘었습니다. 대부분의 환자는 관해 기간 이후에 재발하는 암을 앓고 있습니다. 지금까지 초기 치료 후 종양이 사라진 소수의 환자는 재발하지 않았습니다.
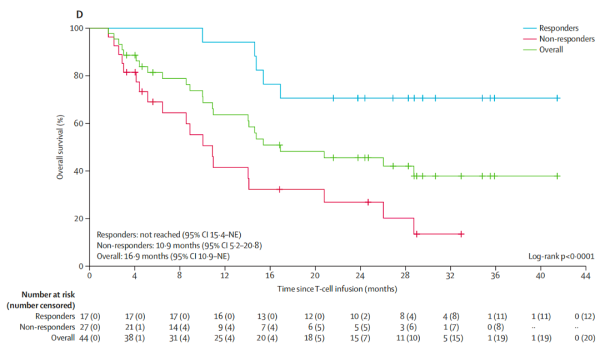
전체 환자 중 평균 생존기간은 15개월 남짓이었고, 1년 생존율은 60%에 달했습니다. 종양이 초기 치료에 완전 반응(즉, 단일 치료 후 종양이 완전히 사라진)을 보인 활막육종 환자의 경우 1년 생존율은 90%, 2년 생존 확률은 70%였습니다.
이 치료의 가장 흔한 부작용은 적혈구 및 백혈구 수가 감소하는 것인데, 이는 조작된 T 세포를 수용할 수 있도록 신체를 준비하는 데 필요한 화학요법으로 인해 발생합니다. 많은 환자들이 T세포 치료의 일반적인 부작용인 사이토카인 방출 증후군을 조절하기 위한 치료가 필요합니다. 추적 기간 동안 발생한 28명의 사망은 모두 치료보다는 암의 궁극적인 진행으로 인한 것으로 확인됐습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.