2025년 CAR-T 연구 및 논문 발표
페이지 정보
작성자 PnH 조회91회 작성일 25-03-31 19:27본문
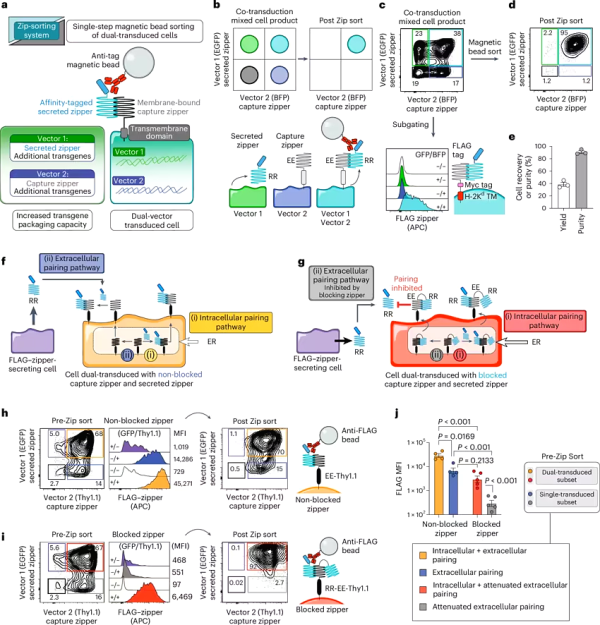
1.Nature Biomedical Engineering:Leucine zipper-based immunomagnetic purification of CAR T cells displaying multiple receptors
키메라 항원 수용체(CAR) T세포 치료에 대한 저항은 종종 여러 가지 메커니즘을 통해 발생하는데, 그 중 가장 분명한 것은 항원 손실과 종양 유발 면역 억제입니다.
최근 국제 학술지 Nature Biomedical Engineering 에 게재된 "Leucine zipper-based immunomagnetic purification of CAR T cells displaying multiple receptors" 라는 제목의 연구 보고서에서 메모리얼 슬론 케터링 암 연구 센터와 다른 기관의 과학자들은 키메라 항원 수용체 T 세포 치료(CAR-T 세포 치료)에 대한 저항 메커니즘을 극복하도록 도울 수 있는 기능을 T 세포에 추가하는 새로운 방법을 연구를 통해 개발했습니다.
오늘날 CAR-T 세포 요법은 암 치료에 혁명을 일으켰고 일부 혈액암 환자에게 강력한 치료 옵션을 제공했습니다. 그러나 어떤 요법도 완벽하지 않으며 일부 환자는 CAR-T 세포 요법에 어느 정도 내성을 갖습니다. 스콧 E. 제임스 교수는 "역사적으로 이 분야의 사람들은 종양이 면역 요법 공격을 회피하기 위해 사용하는 개인화된 전략을 극복하려고 노력했습니다. 현재 벡터 시스템의 제한된 DNA 패키징 용량으로 인해 여러 전략에 저항하도록 T 세포를 조작하는 것은 항상 큰 도전이었습니다. 이 연구에서 우리는 T 세포에서 여러 특성의 인코딩을 촉진할 수 있는 새로운 방법을 개발하여 동시에 여러 종양 탈출 메커니즘을 극복하는 것을 목표로 합니다."라고 말했습니다.
공동 연구를 통해 연구자들은 이중 벡터 접근법을 사용하여 유전 정보 용량을 두 배로 늘리는 시스템을 설계했으며, 이는 동시에 여러 항원을 표적으로 삼을 수 있습니다. 이 시스템은 또한 스위치 수용체를 사용할 수 있게 하는데, 이는 암 세포의 음성 신호를 양성 신호로 변환하여 종양 탈출의 또 다른 메커니즘인 T 세포 고갈을 줄일 수 있습니다. 이 방법은 현재 최대 4개의 항원과 3개의 스위치 수용체에서 테스트되었으며, 더 나은 항종양 활성을 보였습니다. 즉, T 세포가 더 많이 증식하고 더 오래 살 수 있습니다. 연구자들은 이를 zip-sorting 시스템이라고 명명했으며, 이는 새로운 세포 치료법을 구축하고 비교하는 강력한 방법을 제공할 수 있습니다.
2. Nature Communications:CRISPR/Cas9 editing of NKG2A improves the efficacy of primary CD33-directed chimeric antigen receptor natural killer cells
현재 인간에게는 많은 형태의 혈액암이 있으며, 이를 통틀어 백혈병이라고 합니다. 급성 골수성 백혈병(AML)은 흔한 백혈병의 한 형태입니다. 이 병의 주요 특징은 환자의 초기 혈액 세포 전구체(즉, 줄기 세포와 줄기 세포에서 발달한 전구 세포)가 분해되는 것입니다. 이 유형의 백혈병 환자는 집중적인 화학 요법을 받지만, 진단 및 치료 후 5년 동안 생존하는 사람은 20%-50%에 불과합니다. 이 질병을 복잡하게 만드는 것은 이러한 집중적인 요법이 신체의 조혈 줄기 세포 에 파괴적인 영향을 미치며 , 이는 종종 더 심각한 부작용과 관련이 있다는 사실입니다. 이것이 연구자들이 새로운 치료법을 개발해야 하는 절실한 이유입니다.
최근 국제 학술지 Nature Communications 에 게재된 "CRISPR/Cas9 editing of NKG2A improvements the efficiency of primary CD33-directed chimeric antigen receptor natural killer cells" 라는 제목의 연구 보고서에서 , 프랑크푸르트 괴테 대학과 다른 기관의 과학자들은 연구를 통해 CAR-NK 세포를 성공적으로 변형시켰으며, 이는 인간 백혈병과 싸우는 또 다른 대체 방법으로 사용될 가능성이 있습니다. 연구자들은 면역 요법이 숙주의 면역 체계의 자연적인 힘을 이용해 악성 백혈병 세포와 싸울 수 있다고 설명했습니다. 이 요법의 일환으로 암세포는 T세포와 같은 신체 면역 체계의 킬러 세포에 의해 인식될 수 있습니다. 예를 들어, T세포 표면에는 자물쇠와 같은 구조가 있으며, 암세포 표면에 있는 해당 구조를 열쇠처럼 삽입할 수 있습니다. 기술적인 관점에서 T세포의 자물쇠를 "항원 수용체"라고 하고 열쇠를 "항원"이라고 합니다.
열쇠가 자물쇠에 있다면, 즉 항원과 항체가 결합한다면 T 세포는 세포를 죽일 것입니다. 오늘날 연구자들은 항원 수용체를 맞춤화하여 특정 종양 특성을 인식할 수 있습니다. 이를 위해 연구자들은 환자의 혈액에서 T 세포를 정제하고 유전공학 기술을 사용하여 여러 단백질의 특성을 결합하여 특별한 방식으로 특정 종양에 대한 공격을 최적화하는 소위 키메라 항원 수용체(CAR)를 삽입합니다. 키메라 항원 수용체를 갖춘 T 세포(CAR-T 세포)는 현재 인간 백혈병을 치료하는 데 성공적으로 사용되고 있습니다. 현재 사용 중인 또 다른 유형의 킬러 세포는 소위 자연 킬러 세포(NK 세포)입니다. 특정 항원을 통해 악성 세포를 인식하지 않고 다른 표면 이상에 의존합니다. 키메라 항원 수용체가 추가로 추가되면 두 가지 방법으로 암 세포와 싸울 수 있습니다. CAR-NK 세포의 또 다른 장점은 지금까지 임상 연구에서 부작용을 거의 일으키지 않았다는 것입니다.
8. Nature Immunology:Antigen experience history directs distinct functional states of CD8+ CAR T cells during the antileukemia response
키메라 항원 수용체(CAR) T 세포는 B-계열 악성 종양에 대해 효과적으로 보호할 수 있지만, CAR 치료 후 환자에게 질병 재발이 흔하고 다른 종양에 대한 치료 효능은 매우 제한적입니다. 이러한 과제는 CAR-T 세포의 기능을 합리적으로 조작하여 해결할 수 있습니다.
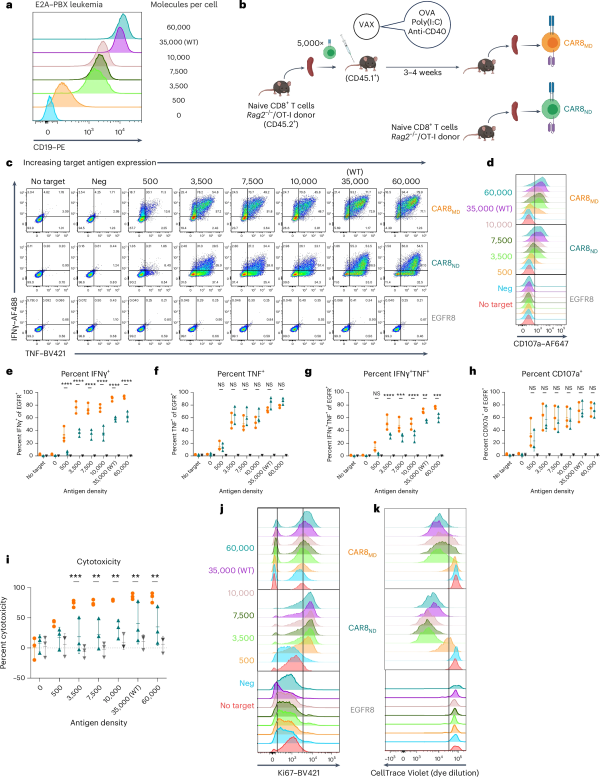
최근 국제 저널 Nature Immunology 에 게재된 "항원 경험 이력은 항백혈병 반응 동안 CD8+ CAR T 세포의 뚜렷한 기능적 상태를 지시한다" 라는 제목의 연구 보고서에서 콜로라도 대학교 Anschutz Medical Campus와 다른 기관의 과학자들은 암과 다른 질병과 싸우는 데 사용되는 일부 CAR-T 세포가 박테리아, 바이러스 및 기타 항원과의 과거 만남에 대한 기억을 가지고 있을 수 있다는 것을 발견했습니다. 이 연구 결과는 과학자들이 더 정확 하고 표적화된 방식으로 세포를 만들도록 촉구할 수 있습니다.
이 기사에서 연구자들은 암, 특히 백혈병과 림프종과 싸우는 효과적인 치료법인 CAR-T 세포에 초점을 맞췄습니다. 면역 세포의 한 유형인 T 세포는 환자의 혈액에서 제거한 다음 암을 표적으로 삼도록 변형하여 환자에게 다시 주입할 수 있습니다. 이제 연구자들은 이들 세포 중 일부가 장기 기억을 가지고 있다는 것을 발견하였고, 과거에 항원에 노출된 적이 있는 CAR-T 세포는 항원에 노출된 적이 없는 세포와 다르게 행동한다는 것을 발견했는데, 이는 세포에 CAR을 삽입하기 위해 광범위한 엔지니어링을 거친 후에도 마찬가지였습니다.
테리 프라이 박사는 대부분의 약물과 달리 CAR-T 세포 제품은 균일하지 않다고 말했습니다. 우리는 변이가 존재한다는 것을 알고 있지만, 이 변이의 본질은 이제 막 이해되기 시작했을 뿐일 수 있습니다. 놀랍게도 항원과의 과거 상호작용은 세포에 지속적인 흔적을 남길 수 있습니다. 연구자들은 이전에 항원을 경험했던 "기억 세포"가 암세포를 빠르게 죽일 수 있지만 동시에 빠르게 지치고 더 느리게 번식할 수 있다는 사실을 발견했는데, 이는 잠재적인 재발의 가능성을 열어줄 수 있습니다. 동시에 연구자들은 항원 경험이 없는 선천 세포의 강력한 확장 및 고갈에 대한 내성과 같은 몇 가지 유리한 질병 저항 능력을 발견했습니다. 연구자들은 두 세포 유형을 직접 비교하여 세포 기능을 조절하고 개선하는 특정 유전자 표적을 식별할 수 있었습니다. 그들은 선천 세포가 RUNX2와 같은 유전자를 표적으로 하여 특별히 향상될 수 있으며, 기억 세포와 비교했을 때 이러한 세포는 수명이 더 길고 더 빨리 번식한다는 것을 발견했습니다.
9. Science Advances:Molecular dynamics at immune synapse lipid rafts influence the cytolytic behavior of CAR T cells
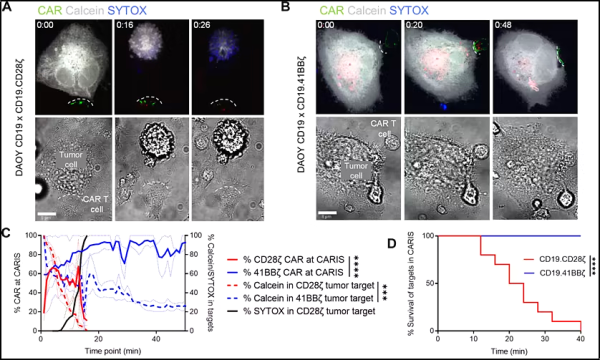
새로운 연구에서 베일러 의과대학, 텍사스 어린이 암 센터, 휴스턴 메소디스트 병원 및 텍사스 어린이 병원의 연구자들은 CAR-T 세포가 암세포에 결합하는 면역 시냅스의 분자 역학이 항암 활동에 어떤 영향을 미치는지 조사했습니다. 이를 위해 그들은 가장 흔한 두 가지 유형의 CAR-T 세포가 암을 죽이는 방식에 대한 새로운 통찰력을 제공했습니다.
관련 연구 결과는 2025년 1월 10일 "면역 시냅스 지질 래프트의 분자 동역학이 CAR T 세포의 세포 용해 행동에 영향을 미친다"라는 제목으로 저널 Science Advances 에 게재되었습니다.
이 연구에서 저자들은 서로 다른 신호 전달 도메인을 가진 CAR-T 세포가 분자 및 세포 수준에서 어떻게 작동하는지 이해하고, CAR-T 세포의 항암 활성을 극대화하는 CAR 분자를 설계하기 위한 기반을 마련하는 것을 목표로 했습니다.
"우리는 두 가지 다른 유형의 CAR-T 세포를 살펴보았습니다." Baylor College of Medicine 및 Texas Children's Cancer Center의 소아 혈액학 및 종양학 교수이자 이 논문의 책임 저자인 Nabil Ahmed 박사가 말했습니다. "첫 번째는 CD28.ζ-CART 세포로, 단거리 선수와 같아 암세포를 빠르고 효과적으로 죽이지만 활동은 짧습니다. 두 번째는 4-1BB.ζ-CART 세포로, 마라톤 선수와 같아 장기간 암세포를 계속 죽입니다."
10. Cancer Immunology Research:TBK1 Targeting Is Identified as a Therapeutic Strategy to Enhance CAR T-Cell Efficacy Using Patient-Derived Organotypic Tumor Spheroids”
오늘날 과학자들은 인간 고형 종양 치료에서 키메라 항원 수용체(CAR) T 세포의 효능을 개선하기 위한 새로운 치료 전략이 필요합니다. 여러 종양 미세환경 요인이 CAR-T 세포 치료에 대한 고형 종양 내성을 촉진하는 것으로 생각되며, 이러한 요인을 식별하고 분석하기 위해 임상적으로 관련성 있는 생물학적 샘플을 사용하는 적절한 모델 시스템은 종종 제한적입니다.
최근 국제 학술지 Cancer Immunology Research 에 게재된 "TBK1 타겟팅은 환자 유래 기관형 종양 구형체를 사용하여 CAR T 세포 효능을 향상시키는 치료 전략으로 확인되었다" 라는 제목의 연구 보고서에서 매사추세츠 종합병원과 다른 기관의 과학자들은 연구를 통해 TBK1 분자가 CAR-T 세포 요법에 대한 내성을 극복하는 열쇠가 될 수 있다는 것을 확인했습니다.
그렇다면 고형 종양이 CAR-T 세포 치료에 저항성을 나타내는 요인은 무엇일까요? CAR-T 세포 요법은 혈액암 환자를 치료하는 데 효과적인 것으로 나타났지만, 종양 미세 환경을 포함한 여러 요인의 영향으로 인해 고형 종양 치료의 효능은 제한적이었습니다. 이를 위해 연구자들은 특수한 종양 3D 미세유체 모델을 사용하여 CAR-T 세포 요법 내성의 메커니즘을 연구했습니다. CAR-T 세포는 고형 종양에서 흔한 항원인 B7-H3를 표적으로 삼도록 설계되었습니다.
사용 가능한 종양 3D 모델은 여러 가지가 있지만, 종양 미세환경의 주요 요소를 충실하게 재현하는 능력은 매우 제한적입니다. 연구자들은 종양 미세환경의 주요 특징을 재현할 수 있는 미세생리학적 3D 모델인 환자 유래 기관형 종양 구형체(PDOTS)를 사용하여 연구자들이 종양과 면역 세포 간의 상호 작용을 분석할 수 있도록 합니다. 연구 결과에 따르면 CAR-T 세포가 표적 세포를 처음 만나면 표면의 억제 수용체 발현이 증가해 기능 장애가 발생 하고 효과가 제한되는 것으로 나타났습니다.
안녕하세요 PnH 입니다
저희 PnH 는 기존의 폐쇄적이고 의존적이였던 암정보에서 벗어나,
원하면 누구나 언제든 찾을 수 있도록 '입증된 암정보의 공개'를 목표로 하고있습니다.
저희 PnH 는 전세계의 암환자분들에게 효과적이고, 입증된 암치료정보를 제공하며
루테시움, CAR-T 카티, TCR-T 티시알티, TIL 틸, 표적치료, 면역치료 등
신뢰도 높은 치료정보와, 검증된 논문을 직접 번역하여 제공하고 있습니다.
(때문에 자료의 불펌은 금지합니다.)
암종별 연구, 치료법, 임상 소식을 누구보다 빠르게 제공해 드리며
환자 스스로 정보를 제대로 알고, 찾고, 이해하실 수 있도록 많은 정보를 제공하기 위해 최선을 다하겠습니다.
감사합니다.